��Ŀ����
����Ŀ������ͨ������ת�����Եõ�C�����·�Ӧ����������ȥ���� ���� ![]() M
M ![]() N��A
N��A ![]() D
D ![]() C
C
A��F�������ʿ��Է�����ͼת����
ע��[O]��ʾ�������������C �����������ķ���Һ��
��1��A�Ĺ����ŵĽṹ��ʽΪ �� �����������������һ������ʯ�ͻ����ķ�չˮƽ��N ����A�ķ�Ӧ����Ϊ �� B��һ��ͬ���칹�������Ϊ ��
��2����д��E����F�����ӷ���ʽ �� ��д��C2H2O2����E�Ļ�ѧ����ʽ��[O]Ϊ��ͭ���ʣ� ��
��3��C��Eһ�������·�Ӧ������������Է���������С�����ʵ�Ħ������Ϊ ��
��4��H���Ӻ���4��̼����ΪC2H2O2��ͬϵ�H��ͬ���칹���к��� ![]() ������״�ṹ��ͬ���칹�����֣��������������칹��
������״�ṹ��ͬ���칹�����֣��������������칹��
��5�����㻯����G����̼���⡢������Ԫ�أ���Է�������Ϊ110��G����̼���Ʒ�Ӧ��������̼�����Ʒ�Ӧ����G�����������ϵ�һ��ȡ����ֻ��һ�֣���G�Ľṹ��ʽΪ ��
��6����֪�� ![]() �� ����ϩΪ��ʼԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳ������ᣬд���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л�����ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������
�� ����ϩΪ��ʼԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳ������ᣬд���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л�����ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������
���𰸡�
��1��![]() ��Ũ���ᡢ170�棻��ȩ
��Ũ���ᡢ170�棻��ȩ
��2��5HOOC��COOH+2MnO4��+16H+=2Mn2++10CO2��+8H2O��OHC��CHO+4Cu��OH��2 ![]() HOOC��COOH+4Cu2O��+4H2O
HOOC��COOH+4Cu2O��+4H2O
��3��134g/mol
��4��8
��5��![]()
��6���⣺��ϩ��HBr�����ӳɷ�Ӧ����CH3CH2Br��Ȼ����ˮ�ⷴӦ����CH3CH2OH���ٷ���������Ӧ����CH3CHO��2������ȩ�����ӳɷ�Ӧ���� ![]() ������Ũ������������·�����ȥ��Ӧ����CH3CH=CHCHO���������������ӳɷ�Ӧ����CH3CH2CH2CH2OH����KMnO4�����·���������Ӧ��������CH3CH2CH2COOH���ϳ�·������ͼΪ��CH2=CH2
������Ũ������������·�����ȥ��Ӧ����CH3CH=CHCHO���������������ӳɷ�Ӧ����CH3CH2CH2CH2OH����KMnO4�����·���������Ӧ��������CH3CH2CH2COOH���ϳ�·������ͼΪ��CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH
CH3CH2OH ![]() CH3CHO
CH3CHO ![]()
![]()
![]() CH3CH=CHCHO
CH3CH=CHCHO ![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH ![]() CH3CH2CH2COOH���ʴ�Ϊ��CH2=CH2
CH3CH2CH2COOH���ʴ�Ϊ��CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH
CH3CH2OH ![]() CH3CHO
CH3CHO ![]()
![]()
![]() CH3CH=CHCHO
CH3CH=CHCHO ![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH ![]() CH3CH2CH2COOH
CH3CH2CH2COOH
���������⣺��1��AΪCH2=CH2 �� �����ŵĽṹ��ʽΪ ![]() ��N����A���Ҵ���Ũ���ᡢ170�������·�����ȥ��Ӧ������ϩ��BΪ
��N����A���Ҵ���Ũ���ᡢ170�������·�����ȥ��Ӧ������ϩ��BΪ ![]() ������һ��ͬ���칹��ΪCH3CHO������Ϊ��ȩ�����Դ��ǣ�
������һ��ͬ���칹��ΪCH3CHO������Ϊ��ȩ�����Դ��ǣ� ![]() ��Ũ���ᡢ170�棻��ȩ����2����E����F�����ӷ���ʽΪ��5HOOC��COOH+2MnO4��+16H+=2Mn2++10CO2��+8H2O����C2H2O2����E�Ļ�ѧ����ʽ��[O]Ϊ��ͭ���ʣ���OHC��CHO+4Cu��OH��2
��Ũ���ᡢ170�棻��ȩ����2����E����F�����ӷ���ʽΪ��5HOOC��COOH+2MnO4��+16H+=2Mn2++10CO2��+8H2O����C2H2O2����E�Ļ�ѧ����ʽ��[O]Ϊ��ͭ���ʣ���OHC��CHO+4Cu��OH��2 ![]() HOOC��COOH+4Cu2O��+4H2O�� ���Դ��ǣ�5HOOC��COOH+2MnO4��+16H+=2Mn2++10CO2��+8H2O��OHC��CHO+4Cu��OH��2
HOOC��COOH+4Cu2O��+4H2O�� ���Դ��ǣ�5HOOC��COOH+2MnO4��+16H+=2Mn2++10CO2��+8H2O��OHC��CHO+4Cu��OH��2 ![]() HOOC��COOH+4Cu2O��+4H2O����3��C��HOCH2CH2OH����E��HOOC��COOH��һ�������·�Ӧ������������Է���������С������Ϊ�Ҷ����Ҷ������������ʵ�Ħ������Ϊ134g/mol�����Դ��ǣ�134g/mol����4��H���Ӻ���4��̼����ΪC2H2O2��OHC��CHO����ͬϵ���H�ķ���ʽΪC4H6O2 �� H��ͬ���칹���к���
HOOC��COOH+4Cu2O��+4H2O����3��C��HOCH2CH2OH����E��HOOC��COOH��һ�������·�Ӧ������������Է���������С������Ϊ�Ҷ����Ҷ������������ʵ�Ħ������Ϊ134g/mol�����Դ��ǣ�134g/mol����4��H���Ӻ���4��̼����ΪC2H2O2��OHC��CHO����ͬϵ���H�ķ���ʽΪC4H6O2 �� H��ͬ���칹���к��� ![]() ������״�ṹ�������������Ȼ����һ�����1��̼̼˫��������������ͬ���칹���У�CH2=CHCH2COOH��CH3CH=CHCOOH��CH2=C��CH3��COOH��CH2=CHCH2OOCH��CH3CH=CHOOCH��CH2=C��CH3��OOCH��CH2=CHOOCCH3 �� CH2=CHCOOCH3 �� �ʹ���8�֣����Դ��ǣ�8����5���з��㻯����G����̼���⡢������Ԫ�أ�G����̼���Ʒ�Ӧ��������̼�����Ʒ�Ӧ����G�����Ȼ������з��ǻ�����Է�������Ϊ110��ȥ��һ����������C6H5������OH��ʣ������Ϊ110��17��77=16���ʻ�����һ��Oԭ�ӣ���G����1��������2�����ǻ�����G�����������ϵ�һ��ȡ����ֻ��һ�֣���G����2�����ǻ����ڶ�λ����G�Ľṹ��ʽΪ
������״�ṹ�������������Ȼ����һ�����1��̼̼˫��������������ͬ���칹���У�CH2=CHCH2COOH��CH3CH=CHCOOH��CH2=C��CH3��COOH��CH2=CHCH2OOCH��CH3CH=CHOOCH��CH2=C��CH3��OOCH��CH2=CHOOCCH3 �� CH2=CHCOOCH3 �� �ʹ���8�֣����Դ��ǣ�8����5���з��㻯����G����̼���⡢������Ԫ�أ�G����̼���Ʒ�Ӧ��������̼�����Ʒ�Ӧ����G�����Ȼ������з��ǻ�����Է�������Ϊ110��ȥ��һ����������C6H5������OH��ʣ������Ϊ110��17��77=16���ʻ�����һ��Oԭ�ӣ���G����1��������2�����ǻ�����G�����������ϵ�һ��ȡ����ֻ��һ�֣���G����2�����ǻ����ڶ�λ����G�Ľṹ��ʽΪ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ��
��

 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�����Ŀ������Cu2O���ھ��������Ĵ����ܶ��ܵ���ע����Ϊ��ȡCu2O�����ַ�����
������ | ��̿���ڸ��������»�ԭCuO |
������ | ��ⷨ��2Cu+H2O |
������ | ���£�N2H4����ԭ����Cu��OH��2 |
��1����ҵ�ϳ��÷���II�ͷ���III��ȡCu2O�������÷���I����ԭ���� ��
��2����֪��2Cu��s��+ ![]() O2��g��=Cu2O��s����H=��akJmol��1C��s��+
O2��g��=Cu2O��s����H=��akJmol��1C��s��+ ![]() O2��g��=CO��s����H=��bkJmol��1
O2��g��=CO��s����H=��bkJmol��1
Cu��s��+ ![]() O2��g��=CuO��s����H=��ckJmol��1
O2��g��=CuO��s����H=��ckJmol��1
��I�����ķ�Ӧ��2CuO��s��+C��s��=Cu2O��s��+CO��g����H=kJmol��1 ��
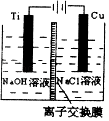
��3������II�������ӽ���Ĥ���Ƶ��Һ��OH����Ũ�ȶ��Ʊ�����Cu2O��װ����ͼ��ʾ���õ�ص�������ӦʽΪ ��
��4������IIIΪ������������Һ̬ƴ��N2H4����ԭ����Cu��OH��2���Ʊ�����Cu2O��ͬʱ�ų�N2 �� ���Ʒ��Ļ�ѧ����ʽΪ ��
��5������ͬ���ܱ������У����������ַ����Ƶõ�Cu2O�ֱ���д��ֽ�ˮ��ʵ�飺 2H2O��g�� ![]() 2H2��g��+O2��g����H��0
2H2��g��+O2��g����H��0
ˮ������Ũ����ʱ��t�仯�����ʾ��
��� | 0 | 10 | 20 | 30 | 40 | 50 | |
�� | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
�� | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
�� | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
����������ȷ����������ĸ���ţ���
A.ʵ���¶ȣ�T1��T2
B.ʵ���ǰ20min��ƽ����Ӧ����v��O2��=7��10��5mol/��Lmin��
C.ʵ��ڱ�ʵ������õĴ���Ч�ʸ�
��6��25��ʱ����50mL0.018mol/L��AgNO3��Һ�м���50mL0.02mol/L���ᣬ���ɳ���������֪Ksp��AgCl��=1.8��10��10 �� ���ʱ��Һ�е�c��Ag+