题目内容
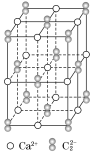
【题目】金属原子在二维空间里的放置有下图所示的两种方式,下列说法中正确的是( )
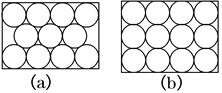
A.图(a)为非密置层,配位数为6
B.图(b)为密置层,配位数为4
C.图(a)在三维空间里堆积可得六方密堆积和面心立方密堆积
D.图(b)在三维空间里堆积仅得简单立方堆积
【答案】C
【解析】
金属原子在二维空间里有两种排列方式,一种是密置层排列,一种是非密置层排列,图1为密置层,图2为非密置层,据此可分析解答。
A.据上述分析,图1为密置层,原子的配位数为6,A选项错误;
B.2为非密置层,非密置层的配位数较密置层小,配位数为4,B选项错误;
C.1为密置层,密置层在三维空间堆积可得到六方最密堆积和面心立方最密堆积两种堆积模型,C选项正确;
D.2为非密置层,非密置层在三维空间堆积可得简单立方堆积和体心立方堆积两种堆积模型,D选项错误;
答案选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀 | I3—溶液中存在平衡: I3— |
B | 在Ca(ClO)2溶液中通入SO2气体,有沉淀生成 | 酸性:H2SO3>HClO |
C | 向淀粉碘化钾溶液中通入过量氯气,溶液由无色变为蓝色,后蓝色褪去 | 氯气具有强氧化性和漂白性 |
D | 在植物油中滴几滴酸性高锰酸钾溶液,振荡,溶液褪色 | 植物油含有酯基 |
A.AB.BC.CD.D
【题目】
废旧可充电电池主要含有Fe、Ni、Cd、Co等金属元素,一种混合处理各种电池回收金属的新工艺如下图所示。
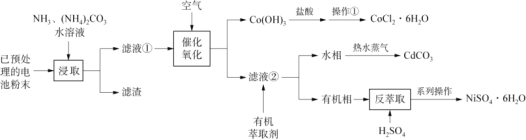
已知:Ⅰ.滤液①中含有Ni(NH3)62+、Cd(NH3)42+、Co(NH3) 62+等物质。
Ⅱ.萃取和反萃取的反应原理分别为:
Ni(NH3)62++ 2HR![]() NiR2+2NH4++4NH3 ;NiR2+2H+
NiR2+2NH4++4NH3 ;NiR2+2H+![]() Ni2+ +2HR
Ni2+ +2HR
(1)为了加快浸取速率,可采取的措施为__________(任写一条)。
(2)已知浸取过程中NH3和NH4+的物质的量之和与Ni、Cd、Co浸取率的关系如表2所示。
表2 浸取过程中氨总量与各离子浸取率的关系
编号 | n(NH3)+ n(NH4+)/mol | Ni浸取率/% | Cd浸取率/% | Co浸取率/% |
① | 2.6 | 97.2 | 88.6 | 98.1 |
② | 3.5 | 86.0 | 98.8 | 86.7 |
③ | 4.8 | 98.4 | 98.8 | 94.9 |
④ | 5.6 | 97.7 | 85.1 | 96.8 |
⑤ | 9.8 | 95.6 | 84.1 | 96.1 |
则可采用的最佳实验条件编号为_____。
(3)Co(OH)3与盐酸反应产生气体单质,该反应的化学方程式______。
(4)操作①的名称为_________、过滤、洗涤。
(5)向有机相中加入H2SO4能进行反萃取的原因为_______(结合平衡移动原理解释)。
(6)将水相加热并通入热水蒸气会生成CdCO3沉淀,并产生使红色石蕊试纸变蓝的气体,该反应的离子方程式为___。
(7)上述工艺流程中可能循环使用的物质为______。
(8)已知Ksp(CdCO3)=1.0×10-12,Ksp(NiCO3)=1.4×10-7。若向物质的量浓度均为0.2mol/L的Cd2+和Ni2+溶液中滴加Na2CO3溶液(设溶液体积增加1倍),使Cd2+恰好沉淀完全,即溶液中c(Cd2+)=1.0×10-5mol/L时,是否有NiCO3沉淀生成(填“是”或者“否”)____。