题目内容
【题目】
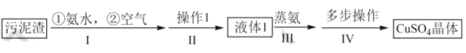
废旧可充电电池主要含有Fe、Ni、Cd、Co等金属元素,一种混合处理各种电池回收金属的新工艺如下图所示。
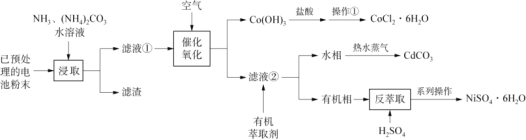
已知:Ⅰ.滤液①中含有Ni(NH3)62+、Cd(NH3)42+、Co(NH3) 62+等物质。
Ⅱ.萃取和反萃取的反应原理分别为:
Ni(NH3)62++ 2HR![]() NiR2+2NH4++4NH3 ;NiR2+2H+
NiR2+2NH4++4NH3 ;NiR2+2H+![]() Ni2+ +2HR
Ni2+ +2HR
(1)为了加快浸取速率,可采取的措施为__________(任写一条)。
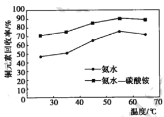
(2)已知浸取过程中NH3和NH4+的物质的量之和与Ni、Cd、Co浸取率的关系如表2所示。
表2 浸取过程中氨总量与各离子浸取率的关系
编号 | n(NH3)+ n(NH4+)/mol | Ni浸取率/% | Cd浸取率/% | Co浸取率/% |
① | 2.6 | 97.2 | 88.6 | 98.1 |
② | 3.5 | 86.0 | 98.8 | 86.7 |
③ | 4.8 | 98.4 | 98.8 | 94.9 |
④ | 5.6 | 97.7 | 85.1 | 96.8 |
⑤ | 9.8 | 95.6 | 84.1 | 96.1 |
则可采用的最佳实验条件编号为_____。
(3)Co(OH)3与盐酸反应产生气体单质,该反应的化学方程式______。
(4)操作①的名称为_________、过滤、洗涤。
(5)向有机相中加入H2SO4能进行反萃取的原因为_______(结合平衡移动原理解释)。
(6)将水相加热并通入热水蒸气会生成CdCO3沉淀,并产生使红色石蕊试纸变蓝的气体,该反应的离子方程式为___。
(7)上述工艺流程中可能循环使用的物质为______。
(8)已知Ksp(CdCO3)=1.0×10-12,Ksp(NiCO3)=1.4×10-7。若向物质的量浓度均为0.2mol/L的Cd2+和Ni2+溶液中滴加Na2CO3溶液(设溶液体积增加1倍),使Cd2+恰好沉淀完全,即溶液中c(Cd2+)=1.0×10-5mol/L时,是否有NiCO3沉淀生成(填“是”或者“否”)____。
【答案】搅拌(适当升温或增大浸取剂的浓度) ③ 2Co(OH)3 +6HCl=2CoCl2 +Cl2↑+6H2O 蒸发浓缩、冷却结晶 根据NiR2+2H+![]() Ni2+ +2HR可知,加入H2SO4使c(H+)增大,平衡向右移动 Cd(NH3)42+ +CO32-
Ni2+ +2HR可知,加入H2SO4使c(H+)增大,平衡向右移动 Cd(NH3)42+ +CO32-![]() CdCO3↓ + 4NH3↑ NH3、有机萃取剂 否
CdCO3↓ + 4NH3↑ NH3、有机萃取剂 否
【解析】
已知已预处理的电池粉末,经过NH3和(NH4)2CO3水溶液的浸取后,得到的滤液①中含有Ni(NH3)62+、Cd(NH3)42+、Co(NH3)62+等物质,在滤液①中通入空气进行催化氧化,得到Co(OH)3沉淀和滤液②,从而将Co元素分离出来,Co(OH)3与盐酸发生氧化还原反应得到CoCl2溶液,再经过蒸发浓缩、冷却结晶、过滤、洗涤得到CoCl26H2O晶体;在滤液②中加入有机萃取剂,发生反应Ni(NH3)62++ 2HR![]() NiR2+2NH4++4NH3,从而将Cd元素与Ni元素分离,水相中含有Cd(NH3)42+,将水相加热并通入热水蒸气会生成CdCO3沉淀;在有机相中加入硫酸进行反萃取,发生反应NiR2+2H+
NiR2+2NH4++4NH3,从而将Cd元素与Ni元素分离,水相中含有Cd(NH3)42+,将水相加热并通入热水蒸气会生成CdCO3沉淀;在有机相中加入硫酸进行反萃取,发生反应NiR2+2H+![]() Ni2+ +2HR,得到NiSO4溶液,再经过蒸发浓缩、冷却结晶、过滤、洗涤得到NiSO46H2O晶体,据此分析解答。
Ni2+ +2HR,得到NiSO4溶液,再经过蒸发浓缩、冷却结晶、过滤、洗涤得到NiSO46H2O晶体,据此分析解答。
(1)搅拌、适当升温或增大浸取剂的浓度,均可加快浸取速率;
(2)通过表2中,浸取过程中氨总量与各离子浸取率的关系数据可知,当n(NH3)+n(NH4+)=4.8mol时,对Ni、Cd、Co浸取率都比较高,因此可采用的最佳实验条件编号为③;
(3)Co(OH)3与盐酸反应生成CoCl2溶液,由此可知Co元素表现了氧化性,则HCl表现还原性,产生的气体单质应为Cl2,根据得失电子守恒,元素守恒可配平该反应的化学方程式为2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O;
(4)CoCl2溶液经过蒸发浓缩、冷却结晶、过滤、洗涤得到CoCl26H2O晶体;
(5)根据以上分析可知,在有机相中加入硫酸进行反萃取,发生反应NiR2+2H+![]() Ni2+ +2HR,得到NiSO4溶液,从平衡移动原理的角度解释,即根据NiR2+2H+
Ni2+ +2HR,得到NiSO4溶液,从平衡移动原理的角度解释,即根据NiR2+2H+![]() Ni2+ +2HR可知,加入H2SO4使c(H+)增大,平衡向右移动,从而得到NiSO4溶液;
Ni2+ +2HR可知,加入H2SO4使c(H+)增大,平衡向右移动,从而得到NiSO4溶液;
(6)水相中含有Cd(NH3)42+、CO32-,将水相加热并通入热水蒸气会生成CdCO3沉淀,并产生使红色石蕊试纸变蓝的气体,则该气体为NH3,则该反应的离子方程式为Cd(NH3)42++CO32-![]() CdCO3↓ +4NH3↑;
CdCO3↓ +4NH3↑;
(7)由以上分析可知,上述工艺流程中可能循环使用的物质为NH3、有机萃取剂;
(8)当Cd2+恰好沉淀完全时,溶液中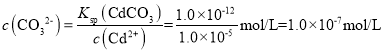 ,此时溶液中,Q(NiCO3)=c(Ni2+)c(CO32-)=0.1×1.0×10-7=1.0×10-8<Ksp(NiCO3),故没有NiCO3沉淀生成。
,此时溶液中,Q(NiCO3)=c(Ni2+)c(CO32-)=0.1×1.0×10-7=1.0×10-8<Ksp(NiCO3),故没有NiCO3沉淀生成。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案