题目内容
【题目】一种新型漂白剂结构如图所示,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列说法正确的是( )
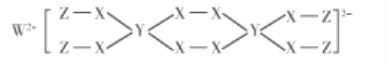
A.非金属性:X>W>Y
B.Y的最高价氧化为对应的水化物为三元酸
C.可利用W与X形成的化合物制备耐高温材料
D.该漂白剂中仅有X均满足8电子稳定结构
【答案】C
【解析】
由题可知,W、Y、Z为不同周期不同主族的短周期元素,说明有一种元素为H,根据图示结构可知,W形成+2价阳离子,X形成2个共价键,Z形成1个共价键,则Z为H元素,W位于ⅡA族,X位于VIA族;W、X对应的简单离子核外电子排布相同,则W为Mg,X为O元素; W、Y、Z的最外层电子数之和等于X的核外层电子数,Y的最外层电子数为6-2-1=3,Y与H、Mg不同周期,则Y为B元素,据此解答。
A.X、W、Y分别为O、Mg、B,其非金属性顺序为:O>B>Mg,即X>Y>W,A错误;
B.Y的最高价氧化为对应的水化物为H3BO3为一元酸,而不是三元酸,B错误;
C.W与X形成的化合物为MgO,其熔点较高,可用于制备耐高温材料,C正确;
D.该漂白剂中O满足8电子稳定结构,而B最外层电子数为3+4=7,不满足8电子稳定结构,D错误;
答案选C。

【题目】碳、氮是中学化学重要的非金属元素,在生产、生活中有广泛的应用。
(1)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管道上安装一个催化转化装置,使NO与CO反应,产物都是空气中的主要成分。写出该反应的热化学方程式___。
已知:①N2(g)+O2(g)=2NO(g) △H=+179.5kJ/mol
②2NO(g)+O2(g)=2NO2(g) △H=-112.3kJ/mol
③NO2(g)+CO(g)=NO(g)+CO2(g) △H=-234kJ/mol
(2)己知植物光合作用发生的反应如下:
6CO2(g)+6H2O(l)![]() C6H12O6(s)+6O2(g) △H=+669.62 kJ/mol
C6H12O6(s)+6O2(g) △H=+669.62 kJ/mol
该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是___。
a.增大CO2的浓度 b.取走一半C6H12O6 c.加入催化剂 d.适当升高温度
(3)N2O5的分解反应2N2O5(g)![]() 4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
C(N2O5)/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
计算在0~2min时段,化学反应速率v(NO2)=___molL-1min-1。
(4)新的研究表明,可以将CO2转化为炭黑进行回收利用,反应原理如图所示。

①在转化过程中起催化作用的物质是___;
②写出总反应的化学方程式___。
(5)工业上以NH3和CO2为原料合成尿素[CO(NH2)2),反应的化学方程式如下:2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(l)根据上述反应,填写下列空白
CO(NH2)2(l)+H2O(l)根据上述反应,填写下列空白
①己知该反应可以自发进行,则△H___0。(填“>”、“<”或“=”);
②一定温度和压强下,若原料气中的NH3和CO2的物质的量之比![]() =x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是___;B点处,NH3的平衡转化率为___。
=x,如图是x与CO2的平衡转化率(α)的关系。α随着x增大而增大的原因是___;B点处,NH3的平衡转化率为___。

③一定温度下,在3L定容密闭容器中充入NH3和CO2,若x=2,当反应后气体压强变为起始时气体压强的![]() 时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=___。
时达到平衡,测得此时生成尿素90g。该反应的平衡常数K=___。