题目内容
20.下列实验方法不科学的是( )| A. | 除去水中含有少量的KNO3:通过蒸馏后收集水 | |
| B. | 检验溶液中的铵根离子:与碱共热,并用湿润的红色石蕊试纸检验产生的气体 | |
| C. | 除去KI固体中的少量碘单质(I2):置于坩埚中加热 | |
| D. | SO42-的检验:溶液先用稀HNO3酸化,然后滴加BaCl2溶液,看是否有沉淀生成 |
分析 A.KNO3不挥发;
B.铵盐能和碱反应生成氨气;
C.碘单质易升华;
D.不能排除SO32-.
解答 解:A.KNO3不挥发,可用蒸馏分离,故A正确;
B.铵盐能和碱反应生成氨气,氨气能使润湿的红色石蕊试纸变蓝色,故B正确;
C.碘单质易升华,碘化钾受热稳定,故C正确;
D.SO32-具有还原性,可被硝酸氧化生成SO42-,不能排除SO32-,故D错误.
故选D.
点评 本题综合考查物质的检验和鉴别的实验设计,为高频考点,题目难度不大,注意把握物质的检验方法,牢固掌握物质的性质为解答该类题目的关键之处.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
10.0.1mol/LNa2S2O3溶液与0.1mol/LH2SO4溶液各5mL和10mL水混合,反应速率为v1mol/(L•s);0.2mol/L Na2S2O3溶液与0.2mol/LH2SO4溶液各5mL和20mL水混合,反应速率为v2mol/(L•s);则v1和v2的关系是( )
| A. | 大于 | B. | 小于 | C. | 等于 | D. | 不能确定 |
11.下列离子方程式书写正确的是( )
| A. | 往石灰乳中通入过量的CO2:OH-+CO2═HCO3- | |
| B. | amol FeBr2溶液中通入amol Cl2:2Fe2++2Br-+2Cl2═Br2+2Fe3++4C1- | |
| C. | 碳酸氢钙溶液加到醋酸中:Ca(HCO3)2+2CH3COOH═Ca2++2CH3COO-+2CO2↑+2H2O | |
| D. | 向50mL 1mol•L-1明矾溶液中滴入数滴0.1mol•L-1Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
8.M、N、X、Y四种物质有如图转化关系(反应条件和其他产物已省略),下列选项不可能的是( )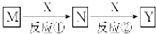

| A. | M:Na X:O2 | B. | M:HNO3 X:Fe | C. | M:NH3 X:O2 | D. | M:Al X:NaOH |
12.某恒温密闭容器中,可逆反应A(s)?B+C(g)△H=+QkJ/mol(Q>O) 达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A. | 保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 | |
| B. | 平衡时,单位时间内c(A)消耗:c(C)消耗=1:1 | |
| C. | 产物B的状态只能为固态或液态 | |
| D. | 若开始时向容器中加入1mol B和1mol C,达到平衡时放出热量QkJ |
9.下列叙述正确的是( )
| A. | 生石灰用作食品抗氧化剂 | |
| B. | Cl2+2Br-═2Cl-+Br2、Zn+Cu2+═Zn2++Cu均为单质被还原的置换反应 | |
| C. | 将KI和FeCl3溶液在试管中混合后,加入CCl4振荡、静置,下层溶液显紫红色,氧化性:Fe3+>I2 | |
| D. | 用含硅胶,铁粉的透气小袋与食品一起密封包装,这个过程不涉及化学变化 |
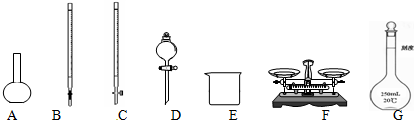
10.下列实验操作说法中,正确的是( )
| A. | 选用酒精作为萃取剂从碘水中萃取碘 | |
| B. | 蒸发操作时,待蒸发皿中的水分完全蒸干后再停止加热 | |
| C. | 在做蒸馏实验时,冷凝器中的水流方向应该与馏分的流动方向相反 | |
| D. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| E. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶中液面下,但不能接触瓶底 | |
| F. | 分液漏斗使用前不需检查是否漏水,但需要用蒸馏水洗涤2-3次 |
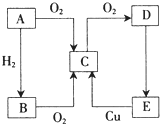 A、B、C、D、E五种物质有如图所示的转化关系,且物质A是一种淡黄色的固体.
A、B、C、D、E五种物质有如图所示的转化关系,且物质A是一种淡黄色的固体.