题目内容
7.如图是CsCl晶体中的一个晶胞,相邻的两个Cs+的核间距为acm,NA为阿伏伽德罗常数,CsCl的相对分子质量用M表示,则CsCl晶体的密度为( )g/cm3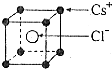
| A. | $\frac{8M}{{N}_{A}•{a}^{3}}$ | B. | $\frac{6M}{{N}_{A}•{a}^{3}}$ | C. | $\frac{4M}{{N}_{A}•{a}^{3}}$ | D. | $\frac{M}{{N}_{A}•{a}^{3}}$ |
分析 该晶胞中Cl-个数为1,Cs+个数=8×$\frac{1}{8}$=1,相邻的两个Cs+的核间距为acm,即其棱长为acm,晶胞体积=a3cm3,晶胞密度ρ=$\frac{m}{V}$,据此分析解答.
解答 解:该晶胞中Cl-个数为1,Cs+个数=8×$\frac{1}{8}$=1,相邻的两个Cs+的核间距为acm,即其棱长为acm,晶胞体积=a3cm3,晶胞密度ρ=$\frac{m}{V}$=$\frac{\frac{M}{{N}_{A}}×1}{{a}^{3}}$g/cm3=$\frac{M}{{a}^{3}{N}_{A}}$g/cm3,故选D.
点评 本题考查基本计算,侧重考查分析计算、空间想象能力,明确密度公式“$\frac{M}{{N}_{A}}×1$”中各个字母的含义是解本题关键,为高考高频点.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
17.下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
| A. | 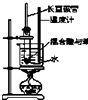 实验室制硝基苯 | B. | 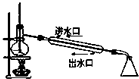 石油分馏 | ||
| C. |  实验室用酒精制取乙烯 | D. | 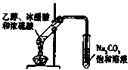 实验室制乙酸乙酯 |
18.设计实验方案是科学探究的重要环节.以下化学实验设计中,能达到实验目的是( )
| A. | 用铜和稀硫酸反应制取硫酸铜溶液 | |
| B. | 用石灰石除去氯化钙溶液中混有的盐酸 | |
| C. | 用氢氧化钠溶液除去二氧化碳中混有的氯化氢气体 | |
| D. | 用酚酞试液检验暴露在空气中的NaOH固体是否变质 |
2.X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构.下列说法正确的是( )
| A. | 原子半径:Z>Y>X | |
| B. | CaX2、CaY2和CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2 | |
| C. | CaY2与水发生氧化还原反应时,CaY2只作氧化剂 | |
| D. | Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点 |
12. 向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
 向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量NaOH溶液中逐滴加AlCl3溶液,生成的沉淀Al(OH)3的质量随AlCl3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | d点对应的溶液中:K+、NH4+、CO32-、I- | |
| B. | c点对应的溶液中:Ag+、Ca2+、NO3-、Na+ | |
| C. | b点对应的溶液中:Na+、S2-、SO42-、Cl- | |
| D. | a点对应的溶液中:Na+、K+、SO42-、HCO3- |
16.三氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
| A. | 三氯化硼液态时能导电而固态时不导电 | |
| B. | 三氯化硼加到水中使溶液的pH升高 | |
| C. | 三氯化硼分子呈正三角形,属非极性分子 | |
| D. | 分子中所有原子都满足最外层8电子稳定结构 |
18.下列有关苯酚钠溶液的叙述,正确的是( )
| A. | 该溶液呈碱性的原因是:C6H5O-+H2O=C6H5OH+OH- | |
| B. | 与少量CO2反应的离子方程式为:2C6H5O-+CO2+H2O=2C6H5OH+CO32- | |
| C. | 25℃时,该溶液中由水电离出的氢离子浓度大于1×10-7mol•L-1 | |
| D. | 该溶液中可能大量存在:K+、SO42-、Cl2、H+ |
