题目内容
【题目】某100 mL无色溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)
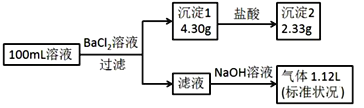
下列说法不正确的是( )
A. 原溶液一定存在CO32-和SO42-,一定不存在Fe3+
B. 若原溶液中不存在Na+,则c(Cl-)<0.1mol·L-1
C. 原溶液中c(Cl-) ≥0.1mol·L-1
D. 原溶液一定存在Cl-,可能存在Na+
【答案】B
【解析】加入氯化钡溶液,生成沉淀,一定含有碳酸根或是硫酸根中的至少一种,则该沉淀为BaSO4、BaCO3中的至少一种,沉淀部分溶解于盐酸,所以一定是BaSO4、BaCO3的混合物,一定存在CO32-和SO42-,硫酸钡沉淀是2.33g,物质的量是2.33g÷233g/mol=0.01mol,碳酸根离子的物质的量是(4.32.33)g÷197g/mol=0.01mol,碳酸根和铁离子不共存,一定不存在Fe3+,所得到的滤液中加入氢氧化钠,放出气体,为氨气,一定含有铵根离子,根据元素守恒,铵根离子的物质的量是1.12L÷22.4L/mol=0.05mol,阳离子所带正电荷的物质的量之和为0.05mol,阴离子所带负电荷的物质的量之和为=0.01×2+0.01×2=0.04mol,所以一定存在氯离子,如不含钠离子,则n(Cl-)=0.01mol,所以c(Cl-)=0.1molL-1。如含有钠离子,则n(Cl-)>0.01mol,所以c(Cl-)>0.1molL-1。则A、根据以上分析可知原溶液一定存在CO32-和SO42-,一定不存在Fe3+,A正确;B、若原溶液中不存在Na+,则c(Cl-)=0.1mol·L-1,B错误;C、根据以上分析可知原溶液中c(Cl-)≥0.1mol·L-1,C正确;D、根据以上分析可知原溶液一定存在Cl-,可能存在Na+,D正确,答案选B。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
