题目内容
下列无色溶液中能大量共存离子组的是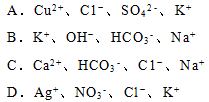
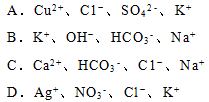
C
按题意要求“无色溶液”,则排除A:Cu2+呈蓝色
B:HCO3-+OH-=CO32-+H2O,排除
C:正确
D:Ag++Cl-=AgCl↓,排除
答案为C
B:HCO3-+OH-=CO32-+H2O,排除
C:正确
D:Ag++Cl-=AgCl↓,排除
答案为C

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
题目内容
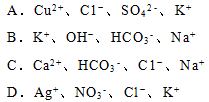

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案