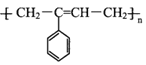
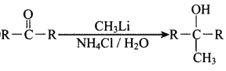题目内容
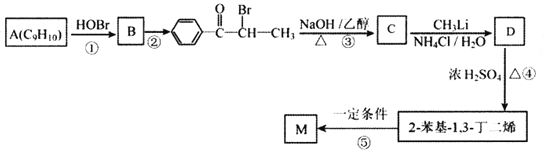
【题目】有机物D,质谱图表明其相对分子质量为86,将8.6gD完全燃烧的产物依次通过装有浓硫酸和碱石灰的装置,浓硫酸中增重9g,碱石灰中增重22g.其相关反应如图所示,其中B、D、E的结构中均含有2个﹣CH3 , 它们的核磁共振氢谱中均出现4个峰.
请回答:
(1)B中所含官能团的名称为;D的分子式为;
(2)Ⅲ的反应类型为(填字母序号);
a.还原反应 b.加成反应 c.氧化反应 d.消去反应
(3)写出下列反应的化学方程式:
Ⅰ:;
Ⅳ﹣:;
(4)C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为;
(5)A的同分异构体中有一对互为顺反异构,且结构中有2个﹣CH3 , 它们的结构简式为和;
(6)E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为 .
【答案】
(1)溴原子,C5H10O
(2)a、b
(3)(CH3)2CHCH2CH2Br+NaOH ![]() (CH3)2CHCH=CH2+NaBr+H2O,(CH3)2CHCH2CHO+2Ag(NH3)2OH
(CH3)2CHCH=CH2+NaBr+H2O,(CH3)2CHCH2CHO+2Ag(NH3)2OH ![]() (CH3)2CHCH2COOH+2Ag↓+4NH3↑+H2O
(CH3)2CHCH2COOH+2Ag↓+4NH3↑+H2O
(4)(CH3)2CHCH2CH2OH+(CH3)2CHCH2COOH ![]() (CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O
(CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O
(5)![]() ,
,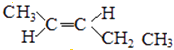
(6)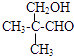
【解析】解:(1)有机物D,质谱图表明其相对分子质量为86,8.6gD该有机物的物质的量为:n= ![]() =
= ![]() =0.1mol,浓硫酸吸收的是水,碱石灰吸收的是二氧化碳,水的物质的量=
=0.1mol,浓硫酸吸收的是水,碱石灰吸收的是二氧化碳,水的物质的量= ![]() =0.5mol,二氧化碳的物质的量=
=0.5mol,二氧化碳的物质的量= ![]() =0.5mol,所以有机物、二氧化碳和水的物质的量之比=0.1mol:0.5mol:0.5mol=1:5:5,所以该有机物分子中含有5个碳原子、10个氢原子,该有机物的相对分子质量是86,86﹣5×12﹣10=16,所以该分子中还含有1个氧原子,其分子式为,C5H10O,D,的结构中含有2个﹣CH3,它的核磁共振氢谱中出现4个峰,说明该有机物中含4种类型的氢原子,则D为(CH3)2CHCH2CHO,由转化关系可知,E为羧酸、C为醇、B为卤代烃,B可在NaOH乙醇溶液加热的条件下反应生成A,B转化为A发生消去反应,则A为烯烃,含有C=C,B、D、E的结构中均含有2个﹣CH3,它们的核磁共振氢谱中均出现4个峰,则C为(CH3)2CHCH2CH2OH,B为(CH3)2CHCH2CH2Br,含有的官能团为溴原子,D的结构简式为:(CH3)2CHCH2CHO,分子式为C5H10O,
=0.5mol,所以有机物、二氧化碳和水的物质的量之比=0.1mol:0.5mol:0.5mol=1:5:5,所以该有机物分子中含有5个碳原子、10个氢原子,该有机物的相对分子质量是86,86﹣5×12﹣10=16,所以该分子中还含有1个氧原子,其分子式为,C5H10O,D,的结构中含有2个﹣CH3,它的核磁共振氢谱中出现4个峰,说明该有机物中含4种类型的氢原子,则D为(CH3)2CHCH2CHO,由转化关系可知,E为羧酸、C为醇、B为卤代烃,B可在NaOH乙醇溶液加热的条件下反应生成A,B转化为A发生消去反应,则A为烯烃,含有C=C,B、D、E的结构中均含有2个﹣CH3,它们的核磁共振氢谱中均出现4个峰,则C为(CH3)2CHCH2CH2OH,B为(CH3)2CHCH2CH2Br,含有的官能团为溴原子,D的结构简式为:(CH3)2CHCH2CHO,分子式为C5H10O,
所以答案是:溴原子;C5H10O;
(2)反应Ⅲ为醛转化为醇,反应为:(CH3)2CHCH2CHO+H2 ![]() (CH3)2CHCH2CH2OH,属于加成反应,与氢气加成反应生成醇,也为还原反应,所以a、b符合条件,
(CH3)2CHCH2CH2OH,属于加成反应,与氢气加成反应生成醇,也为还原反应,所以a、b符合条件,
所以答案是:a、b;
(3)反应Ⅰ为(CH3)2CHCH2CH2Br在乙醇作用下与NaOH反应生成烯烃,为消去反应,方程式为(CH3)2CHCH2CH2Br+NaOH ![]() (CH3)2CHCH=CH2+NaBr+H2O,反应Ⅳ为(CH3)2CHCH2CHO与银氨试剂作用生成羧酸铵、银、氨气、水,为氧化反应,反应的方程式为:(CH3)2CHCH2CHO+2Ag(NH3)2OH
(CH3)2CHCH=CH2+NaBr+H2O,反应Ⅳ为(CH3)2CHCH2CHO与银氨试剂作用生成羧酸铵、银、氨气、水,为氧化反应,反应的方程式为:(CH3)2CHCH2CHO+2Ag(NH3)2OH ![]() (CH3)2CHCH2COOH+2Ag↓+4NH3↑+H2O,
(CH3)2CHCH2COOH+2Ag↓+4NH3↑+H2O,
所以答案是:(CH3)2CHCH2CH2Br+NaOH ![]() (CH3)2CHCH=CH2+NaBr+H2O;(CH3)2CHCH2CHO+2Ag(NH3)2OH
(CH3)2CHCH=CH2+NaBr+H2O;(CH3)2CHCH2CHO+2Ag(NH3)2OH ![]() (CH3)2CHCH2COOH+2Ag↓+4NH3↑+H2O;
(CH3)2CHCH2COOH+2Ag↓+4NH3↑+H2O;
(4)C为(CH3)2CHCH2CH2OH,E为(CH3)2CHCH2COOH,在一定条件下反应生成F,F为有香味的有机化合物,F为酯,所以反应为:(CH3)2CHCH2CH2OH+(CH3)2CHCH2COOH ![]() (CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O,
(CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O,
所以答案是:(CH3)2CHCH2CH2OH+(CH3)2CHCH2COOH ![]() (CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O;
(CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O;
(5)A的同分异构体中有一对互为顺反异构,且结构中有2个﹣CH3,则它们的结构简式为 ![]() 、
、 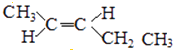 ,
,
所以答案是 ![]() 、
、 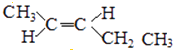 ;
;
(6)E为(CH3)2CHCH2COOH,E的一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,含有﹣CHO与﹣OH,且不能发生消去反应,其结构简式为: 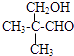 ,
,
所以答案是: 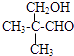 .
.

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】某实验小组学习化学反应速率后,联想到H2O2分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。
编号 | 温度 | 反应物 | 催化剂 |
甲 | 25℃ | 试管中加入3mL5%H2O2溶液 | 1mL蒸馏水 |
乙 | 25℃ | 试管中加入3mL5%H2O2溶液 | 1mL0.1mol/LFeCl3溶液 |
丙 | 40℃ | 试管中加入3mL5%H2O2溶液 | 1mL蒸馏水 |
(1)实验乙中发生反应的化学方程式为_______________。
(2)实验甲和实验乙的实验目的是____________。实验甲和实验丙的实验目的是___________。
(3)实验过程中该同学对实验乙中产生的气体进行收集,并在2min内6个时间点对注射器内气体进行读数,记录数据如下表。
时间/s | 20 | 40 | 60 | 80 | 100 | 120 | |
气体体积/mL | 实验乙 | 15.0 | 29.5 | 43.5 | 56.5 | 69.5 | |
0~20s的反应速率v1=__________mL/s,100~120s的反应速率v2=__________mL/s。不考虑实验测量误差,二者速率存在差异的主要原因是__________。