题目内容
【题目】以芳香化合物A为原料制备灭鼠剂氟鼠酮中间体(G)的一种合成路线如下:
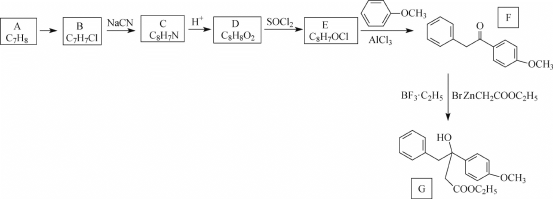
回答下列问题:
(1)A的化学名称是________;A→B的试剂及反应条件依次是________。
(2)E→F的反应类型是________。
(3)D的结构简式为________。
(4)G中的含氧官能团名称为________。
(5)芳香化合物X是F的同分异构体,X能发生银镜反应和水解反应,核磁共振氢谱有4组峰且峰面积之比为6︰6︰1︰1,写出一种符合上述条件的X的结构简式:________。
(6)PES(聚丁二酸乙二醇酯)是一种可生物降解型聚酯,设计以1,2-二氯乙烷为初始原料制备PES的合成路线:________(无机试剂任用)。
【答案】甲苯 Cl2,光照 取代反应 ![]() 羟基、酯基和醚键
羟基、酯基和醚键 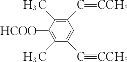 或
或
【解析】
由题干信息可以推出:A: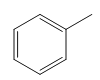 B:
B: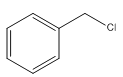 C:
C: D:
D: E:
E: 。
。
(1)A: ,化学名称是甲苯;A:
,化学名称是甲苯;A: B:
B: 取代的是甲基上的氢原子,故试剂及反应条件依次是Cl2,光照;
取代的是甲基上的氢原子,故试剂及反应条件依次是Cl2,光照;
(2)E: 断C-Cl键,剩下的带苯环的结构取代苯甲醚中醚键对位上的氢原子,故E→F的反应类型是取代反应;
断C-Cl键,剩下的带苯环的结构取代苯甲醚中醚键对位上的氢原子,故E→F的反应类型是取代反应;
(3)由分析可知,D的结构简式为 ;
;
(4)芳香化合物X是F的同分异构体,X能发生银镜反应和水解反应,核磁共振氢谱有4组峰且峰面积之比为6︰6︰1︰1,分析一下限定条件:“峰面积之比为6︰6”应该分别是两个甲基对称等效,“X能发生银镜反应和水解反应”说明是甲酸酯。则X的结构简式为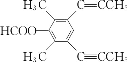 或
或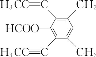 ;
;
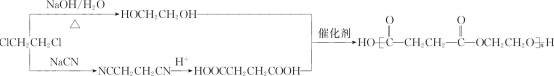
(6)先以1,2-二氯乙烷分别合成丁二酸和乙二醇,丁二酸的合成参照B→D增碳链的方法。最后丁二酸和乙二醇发生缩聚反应生成聚丁二酸乙二醇酯,合成的路线为:
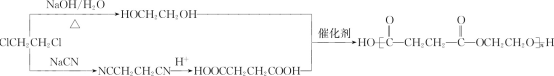 。
。

练习册系列答案
相关题目