题目内容
【题目】“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
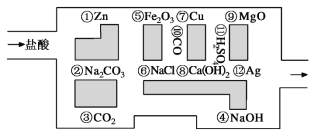
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线):_____________。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有________个,其中能“吃掉”盐酸的盐是________,能“吃掉”盐酸的氧化物有________.
(3)在不能与盐酸反应的物质中,属于氧化物的是______(填写物质序号,下同),属于单质的是____。
(4)如果将盐酸换成氧气,它能沿着盐酸走出的路线“走出”这个迷宫吗?为什么? _________________。
【答案】③⑥⑩⑦ 2 Na2CO3 Fe2O3 和 MgO ③⑩ ⑦ 不能,因为氧气遇到CO等物质会被“吃掉”
【解析】
能和盐酸反应的物质有活泼型排在H前面的金属、金属氧化物、碱、弱酸对应的盐。
(1)图示的物质中能与盐酸反应的有Zn、Fe2O3、MgO、Na2CO3、Ca(OH)2和NaOH,利用图示的物质与盐酸不能反应的物质作出判断即可,由于盐酸不能和二氧化碳、二氧化硫、不活泼金属铜和银、氯化钠、硫酸反应,则连线为③→⑥→⑩→⑦→→;
(2)中和反应是酸与碱反应,根据碱的种类确定中和反应的有个数,碱有2种,则属于酸碱中和反应的有2个能与盐酸反应的盐只有碳酸钠(Na2CO3),反应的离子方程式为CO32-+2H+= CO2↑+H2O;金属氧化物可以与盐酸反应生成盐和水,为Fe2O3 和 MgO;
(3)不能与盐酸反应的物质中,属于氧化物的是CO和CO2;属于单质的是Cu和Ag;
(4)O2可以与CO,Cu、Ag反应,不能沿着盐酸走出的路线“走出”这个迷宫。

【题目】将0.2 mol·L-1的KI溶液和0.05 mol·L-1Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I-![]() 2Fe2++I2”的是
2Fe2++I2”的是
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A. ①和② B. ②和④ C. ③和④ D. ①和③