题目内容
19.室温下,下列溶液中粒子浓度关系正确的是( )| A. | 0.01mol•L-1H2S溶液:c(H+)>c(HS-)>c(S2-)>c(H2S)>c(OH-) | |
| B. | 0.1 mol•L-1NaHSO3溶液:c(Na+)+c(H+)<c(HSO3-)+c(SO32-)+c(OH-) | |
| C. | 等物质的量的NH4Cl和NaCl的混合溶液:c(NH4+)+c(NH3•H2O)+c(Na+)=2c(Cl-) | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-10的Na2CO3溶液:c(HCO3-)+c(H2CO3)=c(10-2-10-12) mol•L-1 |
分析 A.氢硫酸的电离程度较小,主要以第一步为主,则溶液中c(H2S)最大,其次为c(H+),c(OH-)最小;
B.根据亚硫酸氢钠溶液中的电荷守恒判断;
C.根据混合液中的物料守恒判断;
D.该溶液中氢氧根离子浓度为10-2mol/L,氢离子浓度为10-12mol/L,根据质子守恒计算.
解答 解:A.0.01mol•L-1H2S溶液中,硫化氢为二元弱酸,其电离程度较小,主要以第一步为主,则:c(H2S)最大,其次为c(H+),c(OH-)最小,溶液中正确的浓度大小为:c(H2S)>c(H+)>c(HS-)>c(S2-)>c(OH-),故A错误;
B.根据NaHSO3溶液中的电荷守恒可得:c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-),则c(Na+)+c(H+)>c(HSO3-)+c(SO32-)+c(OH-),故B错误;
C.等物质的量的NH4Cl和NaCl的混合溶液中,根据物料守恒可得:c(NH4+)+c(NH3•H2O)+c(Na+)=2c(Cl-),故C正确;
D.该溶液中氢氧根离子浓度为10-2mol/L,氢离子浓度为10-12mol/L,根据质子守恒可得:c(HCO3-)+2c(H2CO3)+c(H+)=c(OH-),则c(HCO3-)+2c(H2CO3)=c(OH-)-c(H+)=c(10-2-10-12) mol•L-1,故D错误;
故选C.
点评 本题考查了离子浓度大小比较,题目难度中等,明确电荷守恒、物料守恒、质子守恒的含义及其应用为解答关键,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.某学习小组用如下装置(支撑仪器略去)探究乙醇的催化氧化反应和乙醛的性质.

(1)实验开始时,对A进行水浴加热,其目的是产生平稳的乙醇气流.
(2)B中反应方程式为CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O.
(3)若装置C中开始发生倒吸,则采取的应急措施是c(填编号).
a.移去图中的酒精灯b.将C中橡皮塞上的短导气管拔出
c.将B尾端的乳胶管取下d.将A与B之间的乳胶管取下,
(4)探究:充分反应后,观察到溴水完全褪色.学习小组通过测定反应前溴水中n(Br2)与反应后溶液中n(Br-)来确定乙醛使溴水褪色的原因.
①假设.请写出假设1的反应类型.
假设1:CH3CHO+Br2→CH2BrCHO+HBr;取代反应
假设2:CH3CHO+Br2→CH3CHBrOBr; 加成反应
假设3:CH3CHO+Br2+H2O→CH3COOH+2HBr. 氧化反应
②结论:若实验测得n(Br2)=0.005mol,n(Br-)=0.01mol,则证明假设3正确.
(5)欲检验乙醇中混有的少量乙醛,甲乙丙三同学设计实验如下表:
则上述方案中你认为能正确完成乙醛的检验的是乙(填甲、乙、丙)

(1)实验开始时,对A进行水浴加热,其目的是产生平稳的乙醇气流.
(2)B中反应方程式为CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O.
(3)若装置C中开始发生倒吸,则采取的应急措施是c(填编号).
a.移去图中的酒精灯b.将C中橡皮塞上的短导气管拔出
c.将B尾端的乳胶管取下d.将A与B之间的乳胶管取下,
(4)探究:充分反应后,观察到溴水完全褪色.学习小组通过测定反应前溴水中n(Br2)与反应后溶液中n(Br-)来确定乙醛使溴水褪色的原因.
①假设.请写出假设1的反应类型.
假设1:CH3CHO+Br2→CH2BrCHO+HBr;取代反应
假设2:CH3CHO+Br2→CH3CHBrOBr; 加成反应
假设3:CH3CHO+Br2+H2O→CH3COOH+2HBr. 氧化反应
②结论:若实验测得n(Br2)=0.005mol,n(Br-)=0.01mol,则证明假设3正确.
(5)欲检验乙醇中混有的少量乙醛,甲乙丙三同学设计实验如下表:
| 试剂、用品 | 预期现象 | |
| 甲 | 酸性高锰酸钾溶液 | 溶液紫红色褪去 |
| 乙 | 溴水 | 溴水褪色 |
| 丙 | 铜丝 酒精灯 | 铜丝由黑色变成光亮的红色 |
2.下列共价化合物中所有原子都满足最外层8电子结构的是( )
| A. | 五氯化磷(PCl5) | B. | 次氯酸(HClO) | C. | 氯化硫(S2Cl2) | D. | 白磷(P4) |
3.如图为番茄电池,下列说法正确的是( )
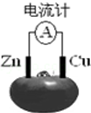

| A. | 锌电极为电池的正极 | |
| B. | 铜电极发生氧化反应 | |
| C. | 工作一段时间后,锌片质量会减轻 | |
| D. | 电池工作时,铜电极附近会出现蓝色 |
 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷. 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基. .
.




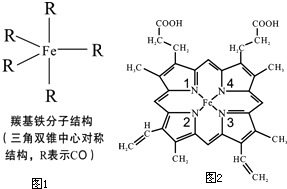 Fe、C、N、O、H可以组成多种物质.回答以下问题:
Fe、C、N、O、H可以组成多种物质.回答以下问题: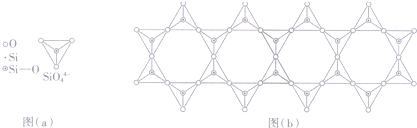
 已知磺酰氯(SO2Cl2)是一种有机氯化剂,SO2(g)+Cl2(g)=SO2C12(g)△H<0,SO2Cl2是一种无色液体,熔点-54.1℃,沸点69.1℃,极易水解,遇潮湿空气会产生白雾.
已知磺酰氯(SO2Cl2)是一种有机氯化剂,SO2(g)+Cl2(g)=SO2C12(g)△H<0,SO2Cl2是一种无色液体,熔点-54.1℃,沸点69.1℃,极易水解,遇潮湿空气会产生白雾.