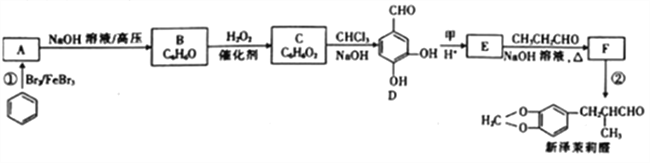
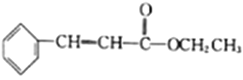
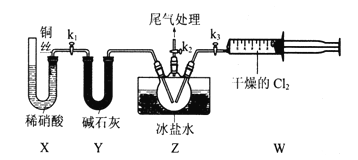
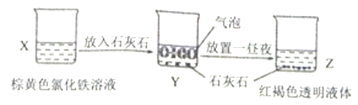
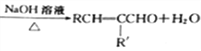题目内容
【题目】25°C时, Ksp (AgCl)= 1.56×10-10, Ksp(Ag2CrO4)= 9.0×10-12,下列说法正确的是
A. AgCl 和 Ag2CrO4 共存的悬浊液中,![]()
B. 向Ag2CrO4悬浊液中加入 NaCl 浓溶液, Ag2CrO4不可能转化为 AgCl
C. 向 AgCl 饱和溶液中加入 NaCl 晶体, 有 AgC1 析出且溶液中 c(Cl-)=c(Ag+)
D. 向同浓度的 Na2CrO4和 NaCl 混合溶液中滴加 AgNO3溶液,AgC1先析出
【答案】D
【解析】A、AgCl 和 Ag2CrO4 共存的溶液中,c(Ag+)是相等的,但由于二者的组成比不同,Ksp的表达式不同,因此c(Cl-)/ c(CO42-)不等于二者的Ksp之比,故A错误;B、根据Ksp的含义,向Ag2CrO4悬浊液中加入NaCl浓溶液,当溶液中c(Cl-) c(Ag+)> Ksp (AgCl)时,就有AgCl沉淀析出,所以B错误;C、向AgCl饱和溶液中加入NaCl晶体,使溶液中c(Cl-)增大,导致c(Cl-) c(Ag+)> Ksp (AgCl),从而析出AgC1,析出沉淀后的溶液中c(Cl-)> c(Ag+),所以C错误;D、向同浓度的Na2CrO4和NaCl混合溶液中滴加AgNO3溶液,根据Ksp计算可得,生成AgCl沉淀需要的c(Ag+)=  =
=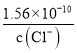 ,生成Ag2CrO4沉淀需要的c(Ag+)=
,生成Ag2CrO4沉淀需要的c(Ag+)= 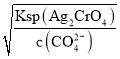 =
= 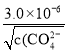 ,前者小于后者,即先析出AgCl沉淀,故D正确。本题正确答案为D。
,前者小于后者,即先析出AgCl沉淀,故D正确。本题正确答案为D。

练习册系列答案
相关题目