题目内容
17.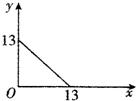 某温度(t℃)下的溶液中,c(H+)=10-xmol•L-1,c(OH-)=10-ymol•L-1,x与y的关系如图所示.请回答下列问题:
某温度(t℃)下的溶液中,c(H+)=10-xmol•L-1,c(OH-)=10-ymol•L-1,x与y的关系如图所示.请回答下列问题:(1)此温度时,水的离子积KW为10-13,则该温度t℃>(填“>”“<”或“=”)25℃.
(2)若将此温度(t℃)下,pH=11的氢氧化钠溶液a L与pH=1的稀硫酸b L混合(假设混合后溶液体积的微小变化忽略不计),若所得混合液pH=2,则a:b=9:2.
(3)已知水存在如下平衡:H2O+H2O?H${\;}_{3}^{+}$O+OH-△H>0,现欲使平衡向右移动,且所得溶液显碱性,选择方法是D.
A.向水中加入NaHSO4固体B.向水中加入NaOH固体
C.加热至100℃D.向水中加入Na
(4)若等pH、等体积的NaOH溶液和氨水分别加水稀释m倍、n倍,稀释后pH相等,则 m<(填“>”“<”或“=”)n.
(5)下列事实一定能说明HNO2是弱电解质的是C
A.用HNO2做导电性实验,灯泡很暗 B.HNO2和NaCl不能反应
C.0.1mol•L-1 HNO2溶液的pH=2.1 D.HNO2溶液稀释pH增大.
分析 (1)由图象可知,x=0时,y=13,y=0时,x=13,则有x+y=13,根据KW=c(H+)×c(OH-)计算;
(2)若将此温度(t℃)下,pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合,此时NaOH溶液中c(OH-)=$\frac{1{0}^{-13}}{1{0}^{-11}}$mol/L=0.01mol/L,稀硫酸溶液中c(H+)=0.1mol/L,
根据反应后溶液的酸碱性判断反应的程度,以此计算;
(3)H2O+H2O?H3O++OH-△H>0,现欲使平衡向右移动,且所得溶液显碱性,说明加入的物质是强碱弱酸盐或消耗氢离子的物质;
(4)pH相等的NaOH和氨水溶液,氨水浓度大于NaOH溶液,加水稀释促进一水合氨电离,NaOH在溶液中完全电离,据此分析;
(5)利用酸不能完全电离或盐类水解的规律来分析HNO2是弱电解质.
解答 解:(1)由图象可知,x=0时,y=13,y=0时,x=13,则有x+y=13,则KW=c(H+)×c(OH-)=(10-xmol•L-1)×(10-y mol•L-1)=10-13 mol2•L-2>10-14 mol2•L-2,
则温度高于常温,
故答案为:10-13;>;
(2)若将此温度(t℃)下,pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合,此时NaOH溶液中c(OH-)=$\frac{1{0}^{-13}}{1{0}^{-11}}$mol/L=0.01mol/L,
稀硫酸溶液中c(H+)=0.1mol/L,则
所得混合液的pH=2,则有$\frac{0.1b-0.01a}{a+b}$=0.01,a:b=9:2;
故答案为:9:2;
(3)酸或碱抑制水电离,含有弱离子的盐促进水电离,H2O+H2O?H3O++OH-△H>0,现欲使平衡向右移动,且所得溶液显碱性,说明加入的物质是强碱弱酸盐或消耗氢离子的物质,Na与水中的氢离子反应生成氢氧化钠,使水的电离平衡向右移动,且所得溶液显碱性;
故答案为:D;
(4)加水稀释促进一水合氨电离,将等体积、等pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水中氢氧根离子浓度大于NaOH,氨水pH大于NaOH溶液,若使稀释后pH相等,氨水稀释倍数应大于氢氧化钠,即m<n,
故答案为:<;
(5)A.用HNO2溶液做导电性实验灯泡很暗,溶液的导电性与离子的浓度有关,弱电解质的浓度大时导电实验中灯泡也很亮,没有对比实验,无法说明HNO2是弱电解质,故A错误;
B.HNO2和NaCl不能发生反应,只能说明不符合复分解反应的条件,但不能说明是弱酸,故B错误;
C.0.1mol•L-1HNO2溶液的pH=2.1,说明亚硝酸部分电离,说明HNO2是弱电解质,故C正确;
D.HNO2溶液稀释pH增大,是因为稀释溶液的体积增大,氢离子浓度减小,不能说明存在电离平衡,即不能说明是弱酸,故D错误;
故答案为:C.
点评 本题考查酸碱混合的定性判断、水的离子积、弱电解质的电离平衡等,题目难度中等,注意水的离子积常数的计算,把握相关计算公式的运用.

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案| A. | 滴加BaC12溶液生成白色沉淀 原溶液中有SO42- | |
| B. | 用洁净铂丝蘸取溶液进行焰色反应:火焰呈黄色 原溶液中有Na+无K+ | |
| C. | 滴加氯水和CC14,振荡、静置.下层溶液显紫色 原溶液中有I- | |
| D. | 滴加几滴稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝 原溶液中无NH4+ |
| A. | 含铅汽油、含磷洗涤剂的使用均可对环境造成危害 | |
| B. | 棉花、木材及草类的纤维都是天然纤维 | |
| C. | 氮化硅陶瓷、光导纤维均属于新型无机非金属材料 | |
| D. | 煤、石油、天然气均属于可再生的化石燃料 |
| A. | 标准状况下,18g水的体积为22.4L | |
| B. | 1mol H2的质量只有在标准状况下才约为2g | |
| C. | 1mol H2和O2的混合气体的体积约为22.4L | |
| D. | 标准状况下,a L氧气和氮气的混合物含有的分子数约为$\frac{a}{22.4}$ NA个 |
| A. | 粗铜在阳极的反应顺序是:Fe-2e-═Fe2+、Ni-2e-═Ni2+、Cu-2e-═Cu2+,杂质金和银不反应形成“阳极泥” | |
| B. | 电解一段时间后,溶液中Cu2+减小 | |
| C. | 若电路中通过1 mol电子,阳极有0.5 mol铜被氧化 | |
| D. | 阴极反应只有Cu2++2e-═Cu |
| A. | 放电时,正极发生的反应是:Pb(s)+SO${\;}_{4}^{2-}$(aq)-2e-═PbSO4(s) | |
| B. | 充电时,每消耗1molPbSO4的同时转移2mol电子 | |
| C. | 放电时,该电池的负极材料是铅板 | |
| D. | 充电时,电池中硫酸的浓度不断变小 |
| A. | 过滤 | B. | 蒸发 | C. | 分液 | D. | 萃取 |
| A. | 32g O2所含的原子数目为NA | |
| B. | 0.5mol H2O含有的原子数目为1.5 NA | |
| C. | 1mol SO2含有的SO2分子数目为NA | |
| D. | 0.5NA个Cl2的物质的量是0.5 mol |