题目内容
5.关于下列装置说法正确的是( )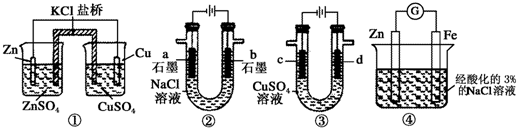
| A. | 装置①中,一段时间后SO42-浓度增大 | |
| B. | 装置②中滴入酚酞,a极附近变红 | |
| C. | 用装置③精炼铜时,c极为粗铜 | |
| D. | 装置④中发生吸氧腐蚀 |
分析 A.装置①是原电池,溶液中SO42-不参加反应;
B.电解时,b是阳极、a是阴极,阳极上生成氯气、阴极上生成氢气,且阴极附近有NaOH生成,溶液呈碱性;
C.电解精炼粗铜时,粗铜作阳极、纯铜作阴极;
D.强酸性条件下,锌发生析氢腐蚀,弱酸性或中性条件下,锌发生吸氧腐蚀.
解答 解:A.装置①是原电池,溶液中SO42-不参加反应,所以放电过程中硫酸根离子浓度不变,故A错误;
B.电解时,b是阳极、a是阴极,阳极上生成氯气、阴极上生成氢气,且阴极附近有NaOH生成,溶液呈碱性,所以a电极附近溶液呈红色,故B正确;
C.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,所以d为粗铜,故C错误;
D.强酸性条件下,锌发生析氢腐蚀,弱酸性或中性条件下,锌发生吸氧腐蚀,该溶液呈强酸性,所以应该发生析氢腐蚀,故D错误;
故选B.
点评 本题以原电池和电解池为载体考查化学实验方案评价,为高频考点,明确实验原理是解本题关键,知道各个电极上发生的反应,注意发生析氢腐蚀和吸氧腐蚀对溶液酸碱性的要求,易错选项是D.

练习册系列答案
相关题目
16.除去乙烷中混有的少量乙烯,正确的处理方法是( )
| A. | 将气体通入水 | B. | 将气体通入澄清石灰水 | ||
| C. | 将气体通入溴水 | D. | 将气体通入氯气进行光照 |
13.设NA为阿伏加德罗常数的值.下列叙述不正确的是( )
| A. | 7.80g Na2O2与5.85g NaCl所含阴离子数均为0.1NA | |
| B. | 一定条件下,1.4g N2与0.2mol H2混合充分反应,转移的电子数为0.3NA | |
| C. | 常温常压下,22.4LNH3所含分子数小于NA | |
| D. | 标准状况下,28g聚乙烯完全燃烧,产生的CO2数为2NA |
20.“化学无处不在”,下列与化学有关的说法不正确的是( )
| A. | 由于甲酸的缘故,人被蜂蚁蜇咬后会感觉疼痛难忍,涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| B. | 用浸过酸性高锰酸钾溶液的硅藻土吸收水果、花朵产生的乙烯,可以延长果实或花朵的成熟期 | |
| C. | 将金属与电源正极相连可有效保护金属不被腐蚀 | |
| D. | 泡沫灭火器利用双水解原理喷出泡沫覆盖在燃烧物品上,使燃着的物质与空气隔离,并降低温度,达到灭火的目的 |
10. 乙二酸俗称草酸是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示)填空:
乙二酸俗称草酸是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示)填空:
(1)写出H2C2O4的电离方程式H2C2O4?H++HC2O4-、HC2O4-?H++C2O42-
(2)KHC2O4溶液显酸性的原因是HC2O4-的电离程度大于水解程度向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是AD
A.c(K+)═c(HC2O4-)+c(H2C2O4)+c(C2O42-) B.c(Na+)═c(H2C2O4)+c(C2O42-)
C.c(K+)+c(Na+)═c(HC2O4-)+c(C2O42-) D.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失.写出反应的离子方程式2MnO4-+5H2C2O4+6H+→2Mn2++10CO2↑+8H2O又知该反应开始时速率较慢,随后大大加快,可能的原因是生成的Mn2+对该反应具有催化作用
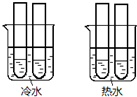
(4)某同学设计实验如图所示:两个烧杯中的试管都分别盛有2ml0.1mol/LH2C2O4溶液和4mL 0.1mol/L 酸性KMnO4溶液,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究温度对反应速率的影响,但该实验始终没有看到溶液褪色,推测原因KMnO4溶液过量.
 乙二酸俗称草酸是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示)填空:
乙二酸俗称草酸是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示)填空:| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(2)KHC2O4溶液显酸性的原因是HC2O4-的电离程度大于水解程度向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是AD
A.c(K+)═c(HC2O4-)+c(H2C2O4)+c(C2O42-) B.c(Na+)═c(H2C2O4)+c(C2O42-)
C.c(K+)+c(Na+)═c(HC2O4-)+c(C2O42-) D.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失.写出反应的离子方程式2MnO4-+5H2C2O4+6H+→2Mn2++10CO2↑+8H2O又知该反应开始时速率较慢,随后大大加快,可能的原因是生成的Mn2+对该反应具有催化作用
(4)某同学设计实验如图所示:两个烧杯中的试管都分别盛有2ml0.1mol/LH2C2O4溶液和4mL 0.1mol/L 酸性KMnO4溶液,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究温度对反应速率的影响,但该实验始终没有看到溶液褪色,推测原因KMnO4溶液过量.
17.下列应用不涉及到盐类水解的是( )
| A. | 用热的纯碱清洗油污 | B. | 氯气难溶于NaCl溶液中 | ||
| C. | 明矾的净水作用 | D. | 泡沫灭火器的使用原理 |
14.在有机分子中,若某个碳原子连接着4个不同的原子或原子团,则这个碳原子被称为“手性碳原子”,凡含有手性碳原子的物质一定具有光学活性.下列物质中无光学活性的是( )
| A. | CH3CH(Br)OH | B. | CH3CH(CH2OH)CHO | ||
| C. | CH3CH2CH(CH3)CH2CH3 | D. | HOOCCH(Br)COOCH3 |
15.电化学在日常生活中有广泛的应用,下列说法或做法正确的是( )
| A. | 暴雨后遭洪水浸泡的铁门生锈是因为发生化学腐蚀 | |
| B. | 白铁皮(铁镀锌)表面有划损时,不能阻止铁被腐蚀 | |
| C. | 废弃的干电池不能随意丢弃,但可以土埋处理 | |
| D. | 不能将铁制自来水管与铜制水龙头连接 |