题目内容
5.把3molA气体和2.5molB气体混合放入2L密闭容器中,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),经5min达到平衡,此时生成1molC,测得D平均反应速率为0.2mol•(L•min)-1,求:(1)平衡时A的物质的量浓度;
(2)x的值.
分析 (1)c(A)平衡=$\frac{n}{V}$,根据平衡时C的物质的量,利用物质的量之比等于化学计量数之比,求出△n(A),再利用n(A)平衡=n(A)起始-△n(A),求出n(A)平衡,代入计算;
(2)根据D的反应速率求出D的物质的量,根据反应的物质的量之比等于化学计量数之比计算x.
解答 解:(1)△n(A)=$\frac{3}{2}$×1mol=1.5mol,
n(A)平衡=n(A)起始-△n(A)=3mol-1.5mol=1.5mol,
所以c(A)平衡=$\frac{1.5mol}{2L}$=0.75mol/L,
答:平衡时A的物质的量浓度为0.75mol/L;
(2)D的物质的量为n(D)=0.2mol•(L•min)-1×5min×2L=2mol,
物质的量之比等于化学计量数之比,所以2:x=1mol:2mol,解得x=4,
答:x的值是4.
点评 本题考查化学平衡的计算,题目难度不大,注意对基础知识的理解、积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3KJ/mol.它表示( )
| A. | 碳与水反应吸收131.3 KJ的热量 | |
| B. | 固态碳和气态水各1mol反应,放出131.3 KJ的热量 | |
| C. | 1mol碳和1mol水反应吸收131.3 KJ的热量 | |
| D. | 1mol固态焦炭与1mol水蒸气反应产生一氧化碳和氢气,吸收131.3 KJ的热量 |
19.实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别是( )
| A. | 1000mL,212g | B. | 950mL,201.4g | C. | 任意规格,212g | D. | 500mL,106g |
17.下列物质中,不含有硅酸盐的是( )
| A. | 水玻璃 | B. | 太阳能电池 | C. | 黏土 | D. | 普通水泥 |
15.设NA表示阿伏加德罗常数数值,下列说法正确的是( )
| A. | NA个氢气分子所占的体积为22.4L | |
| B. | 2NA个二氧化碳分子的质量为44g | |
| C. | 1000mL0.1mol/L的NaCl溶液中,Na+和Cl-离子总数为0.2NA | |
| D. | 17g氨气中所含原子数为4NA |
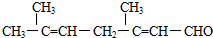 ,若要检验出其中的碳碳双键,方法是先加足量的银氨溶液使醛基氧化,然后再加入酸性的KMnO4溶液,若酸性KMnO4溶液的紫色褪去,证明有碳碳双键存在.
,若要检验出其中的碳碳双键,方法是先加足量的银氨溶液使醛基氧化,然后再加入酸性的KMnO4溶液,若酸性KMnO4溶液的紫色褪去,证明有碳碳双键存在.