题目内容
【题目】某小组探究“地康法制氯气”的原理并验证Cl2的性质,设计实验如下(夹持装置略去)请回答下列问题:
I. Cl2的制备。
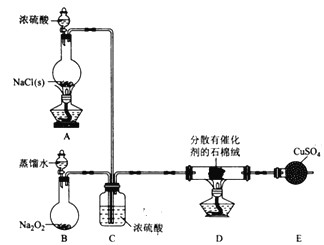
(1)装置B中发生反应的化学方程式为 ________________________________。
(2)装置C的作用除干燥气体外还有_______________________。
(3)装置 E中盛放CuSO4的仪器名称为_______________;反应开始后,硫酸铜变蓝,则装置D中发生反应的化学方程式为 _______________________________。
II.Cl2性质的验证。
该小组用实验I中制得的Cl2和如图所示装置(不能重复使用)依次验证干燥纯净的Cl2无漂白性、湿润的Cl2有漂白性、Cl的非金属性强于S
査阅资料:
①PdCl2溶液捕获CO时,生成金属单质和两种酸性气体化合物;
②少量CO2不干扰实验;
③该实验条件下,C与Cl2不反应。
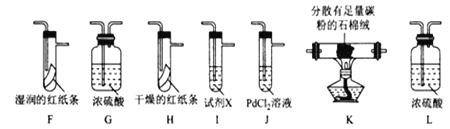
(4)按气流从左到右的方向,装置连接的合理顺序为E→ → → → → → → →尾气处理(填装置字母)________________。
(5)试剂X的名称为________________。
(6)装置J中发生反应的化学方程式为______________________________________。
【答案】2Na2O2+2H2O=4NaOH+O2 控制气体的流速和比例、使气体混合均匀 (球形)干燥管 4HC1+O2![]() 2H2O+ 2C12 G(或L)KJL(或G )HFI 硫化钠溶液 PdCl2+CO+H2O=Pd+CO2+2HC1
2H2O+ 2C12 G(或L)KJL(或G )HFI 硫化钠溶液 PdCl2+CO+H2O=Pd+CO2+2HC1
【解析】
Ⅰ. (1)装置B中为过氧化钠与水反应生成氢氧化钠和氧气,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑;综上所述,本题答案是:2Na2O2+2H2O=4NaOH+O2↑。
(2)装置C的作用除干燥气体外,还可以通过调节单位时间内的气泡数,控制气体的流速和比例、使气体混合均匀的作用;综上所述,本题答案是:控制气体的流速和比例、使气体混合均匀。
(3)由装置图可知,盛放CuSO4的仪器为(球形)干燥管;由信息知,加热条件下,HC1与O2反应生成氯气和水,可得方程式:4HC1+O2![]() 2H2O+ 2C12;综上所述,本题答案是:(球形)干燥管; 4HC1+O2
2H2O+ 2C12;综上所述,本题答案是:(球形)干燥管; 4HC1+O2![]() 2H2O+ 2C12 。
2H2O+ 2C12 。
II.(4)制得的Cl2中混有水蒸气、O2、HCl,用浓硫酸除去水蒸气,足量碳粉除去O2,生成的CO用PdCl2除去,同时HCl溶解于水中,且可溶性金属氯化物的溶液可降低Cl2的溶解度,再通过浓硫酸除去水蒸气;净化后的Cl2分别通过干燥的红纸条、湿润的红纸条、Na2S溶液,以验证Cl2的性质;所以装置的顺序应为E→G(或L)→K→J→L(或G)→H→F→I;综上所述,本题答案是:G(或L)KJL(或G )HFI。
(5)可用盐溶液中的置换反应来验证元素非金属性的强弱,氯气与硫化钠溶液反应生成单质硫,黄色沉淀,所以试剂X可以选用硫化钠溶液;综上所述,本题答案是:硫化钠溶液。
(6)装置J中发生的是PdCl2溶液捕获CO的反应,由信息可得方程式:PdCl2+CO+H2O=Pd+CO2+2HC1;综上所述,本题答案是:PdCl2+CO+H2O=Pd+CO2+2HC1。

 优百分课时互动系列答案
优百分课时互动系列答案【题目】在实验室中可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①为氯气发生装置;②的试管里盛有15 mL 30%KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有________(填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水
C.浓硫酸 D.饱和碳酸氢钠溶液
(2)本实验中制取次氯酸钠的离子方程式是_______________________。
(3)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
实验现象 | 原因 |
溶液最初从紫色逐渐变为___________色 | 氯气与水反应生成的H+使石蕊变色 |
随后溶液逐渐变为无色 | ___________________________ |
然后溶液从无色逐渐变为_________色 | ____________________________ |