题目内容
【题目】海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示。下列说法不正确的是( )

A. 可用BaCl2溶液除去粗盐中的SO42-
B. 从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2===2Cl-+Br2
C. 试剂1可以选用石灰乳
D. 工业上,电解熔融Mg(OH)2冶炼金属镁
【答案】D
【解析】
A.氯化钡和硫酸根离子反应生成难溶性的硫酸钡,且氯离子不是杂质离子,故A正确;
B.氯气能将溴离子氧化为溴单质,然后采用萃取的方法从溶液中获取溴,故B正确;
C.煅烧贝壳得到CaO,将CaO溶于水得到石灰乳,石灰乳和镁离子反应生成氢氧化镁沉淀,试剂1廉价且原料来源广泛,故C正确;
D.氢氧化镁受热分解,工业上采用电解熔融氯化镁的方法冶炼镁,故D错误;
答案:D

【题目】Ⅰ、A、B是两种常见的无机物,它们分别能与下图中周围4种物质在一定条件下反应:
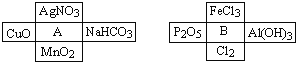
请回答下列问题:
(1)A溶液与B溶液反应的离子方程式 ______ .
(2)若A与其周围某物质在一定条件下反应,产物之一是B周围的一种,则此反应的离子方程式为 ______
(3)在A、B周围的8种物质中,有些既能与A反应又能与B反应.则这些物质可能是: ______ .
Ⅱ、在Na+浓度为0.6mol/L的某澄清溶液中,还可能含有表中的若干种离子:
阳离子 | K+、Ag+、Mg2+、Ba2+ |
阴离子 | NO3-、CO32-、SO42-、SiO32- |
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
Ⅲ | 在Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
试回答下列问题:
(1)实验I中生成沉淀的离子方程式为______。
(2)实验Ⅱ中判断沉淀是否洗涤干净的操作为:______。
(3)通过实验I、Ⅱ、Ⅲ和必要计算,判断K+______ 一定存在(填“是”或“否”),若存在,其最小浓度为______。(若不存在,此空不需填写)