题目内容
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温常压下,22.4 L CH4中含有4 nA个C-H键 |
| B.1 mol Fe与足量稀硝酸反应,转移2 nA个电子 |
| C.0.5 mol·L-1 FeCl3溶液中含有1.5 nA个Cl- |
| D.常温下,22g CO2含有nA个氧原子 |
D
解析试题分析:A、常温常压下,22.4 L CH4的物质的量不是1mol,其中含有的C-H键个数不是4nA,A不正确;B、硝酸是强氧化性酸,能把铁氧化生成铁离子,因此1 mol Fe与足量稀硝酸反应,转移3 nA个电子,B不正确;C、0.5 mol·L-1 FeCl3溶液的体积不能确定,不能计算氯离子的个数,C不正确;D、常温下,22g CO2的物质的量=22g÷44g/mol=0.5mol,含有2×0.5=1nA个氧原子,D正确,答案选D。
考点:考查阿伏伽德罗常数的有关计算

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,pH=2的H2SO4溶液中含有的H+离子数目为0.01NA |
| B.当H2O与Na2O2反应生成1 molO2时,转移的电子数目为4NA |
| C.标准状况下,2.24 L CO和CO2混合气体中含有的碳原子数为0.1NA |
| D.1 L 0.1 mol·L-1 FeCl3溶液中含有的Fe3+离子数目为0.1NA |
设NA为阿伏伽德罗常数的数值,则下列说法中,正确的是
A.常温下,0.1mol碳酸钠晶体中含有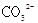 的个数为0.1NA 的个数为0.1NA |
| B.标准状况下,11.2L苯含有C-H键数目为3NA |
| C.常温常压下,54 g重水(D2O)含水分子数为3NA |
| D.将NA个Cl2分子通入足量的水中,所转移的电子总数为NA |
NA表示阿伏加德罗常数,下列说法正确的是
| A.常温常压下,32g O2含有的原子数为2NA |
| B.100mL 1mol·L-1氨水中,含有OH- 离子数是0.1 NA |
| C.100mL 2 mol·L-1碳酸钠溶液中,CO2-3离子数为0.2NA |
| D.标准状况下,22.4LCl2通入足量NaOH溶液,转移的电子数为2NA |
将51.2g铜恰好完全溶于一定量的硝酸溶液中,得到硝酸铜溶液,收集到氮的氧化物(含NO、NO2、N2O4)的混合物共17.92L(标准状况),在这些气体中通入VL(标准状况)的氧气后用一定量的氢氧化钠溶液吸收,结果剩余2.24L(标准状况)气体。则通入氧气的体积V为
| A.7.28L | B.8.96L | C.11.20L | D.16.8L |
在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子,同时含有NA个金属离子。则该硫酸盐的物质的量浓度为(NA表示阿佛加德罗常数的值)
| A.1mol·L-1 | B.2.5 mol·L-1 | C.5 mol·L-1 | D.2 mol·L-1 |
下列说法不正确的是
| A.在一定条件下,催化分解80g SO3,混合气体中氧原子数为3×6.02×1023 |
| B.一定条件下,铁与水蒸气反应生成8.96L H2时(已折合成标况),转移的电子数为0.8×6.02×1023 |
| C.100mL 1mol/L AlCl3与3mol/L NaCl的混合溶液中,Cl— 的个数为0.6×6.02×1023 |
| D.含有非极性键的数目为6.02×1023的Na2O2与水充分反应,标况下产生O2 22.4L |
v L Fe2(SO4)3溶液中含有a g SO42-,取此溶液0.5v L,用水稀释至2v L,则稀释后溶液中Fe3+的物质的量浓度为
A.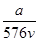 mol·L-1 mol·L-1 | B.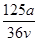 mol·L-1 mol·L-1 |
C.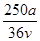 mol·L-1 mol·L-1 | D.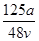 mol·L-1 mol·L-1 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A.S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA |
| B.将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积约为22.4L |
| C.在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2转移的电子数为8NA |
| D.100ml1mol/LAlCl3溶液中含的阳离子数为0.1NA |