题目内容
将几滴KSCN(SCN-是“类卤离子”,与氯离子性质相似)溶液加入酸性的含有Fe3+的溶液中,溶液变成血红色。将该红色溶液分为两份,①一份中加入适量KMnO4溶液,红色褪去;②向另一份中通入SO2,红色也褪去。
下列说法不正确的是
| A.①红色褪去的原因可能是KMnO4将SCN-氧化,使[Fe(SCN)]2+消失 |
| B.[Fe(SCN)]2+中Fe3+与SCN-以配位键结合。 |
| C.②红色褪去的原因是SO2具有漂白性 |
| D.SCN-在适当条件下可失去电子被氧化剂氧化为(SCN)2 |
C
解析试题分析:A.①在溶液中存在平衡:Fe3++3SCN- Fe(SCN)3. KMnO4有强氧化性,当滴入KMnO4溶液时,KMnO4将SCN-氧化为(SCN)2,平衡逆向移动,红色物质逐渐减少,因此红色褪去。正确。B.在Fe3+中存在空轨道,在SCN-的S原子上存在孤对电子,所以[Fe(SCN)]2+中Fe3+与SCN-以配位键结合。正确。C.②红色褪去的原因是因为发生反应:SO2+2Fe3++2H2O=2Fe2++4H++SO42-.错误。D.SCN-有还原性,在适当条件下当遇到强氧化剂时可失去电子被氧化剂氧化为(SCN)2。正确。
Fe(SCN)3. KMnO4有强氧化性,当滴入KMnO4溶液时,KMnO4将SCN-氧化为(SCN)2,平衡逆向移动,红色物质逐渐减少,因此红色褪去。正确。B.在Fe3+中存在空轨道,在SCN-的S原子上存在孤对电子,所以[Fe(SCN)]2+中Fe3+与SCN-以配位键结合。正确。C.②红色褪去的原因是因为发生反应:SO2+2Fe3++2H2O=2Fe2++4H++SO42-.错误。D.SCN-有还原性,在适当条件下当遇到强氧化剂时可失去电子被氧化剂氧化为(SCN)2。正确。
考点:考查影响络合平衡的知识。

 名校课堂系列答案
名校课堂系列答案在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)  Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2。下列说法正确的是
Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2。下列说法正确的是
| A.恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,Ni(CO)4的百分含量将增大 |
| B.在80 ℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v(正)<v(逆) |
| C.恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 |
| D.上述生成Ni(CO)4(g)的反应为吸热反应 |
下列四种X溶液,均能跟盐酸反应,其中反应最快的是
| A.10℃ 20mL 3mol/L的X溶液 | B.20℃ 30mL 2molL的X溶液 |
| C.20℃ 10mL 4mol/L的X溶液 | D.10℃ 10mL 2mol/L的X溶液 |
在2L密闭容器中,保持恒温,加热KClO3和MnO2固体混合物制取O2,5min后,生成O232克,则此反应的平均速率可表示为( )
| A.v(O2)=3.2g·L-1·min-1 | B.v(O2)=0.1 mol·L-1·min-1 |
| C.v(KCl)=0.1 mol·L-1·min-1 | D.v(KClO3)=0.0667 mol·L-1·min-1 |
对可逆反应4NH3(g)+ 5O2(g)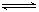 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
| A.达到化学平衡时,υ正=υ逆=0 |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态 |
| C.达到化学平衡时,若增大容器体积,则正反应速率减少,逆反应速率增大 |
| D.达到化学反应平衡后,改变条件当υ正>υ逆,平衡向正反应方向移动 |
可逆反应2NO2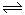 2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n molNO
②单位时间内生成n mol O2的同时生成2n molNO2
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
| A.①④ | B.②④ | C.①③④ | D.①②③④⑤ |
-定条件下,在体积为VL的密闭容器中发生如下反应 一段时间后达到化学平衡状态。改变某一条件,下列说法正确的是
一段时间后达到化学平衡状态。改变某一条件,下列说法正确的是
| A.若升高温度,反应混合气体密度不变时即达到新平衡状态 |
| B.若增大B的浓度,△H减小 |
| C.若使用适当催化剂,A的转化率增大 |
| D.若增大压强,平衡向右移动,则m+n>p+q |
下列各图与表述不一致的是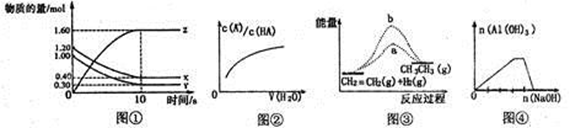
| A.图①表示T℃时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线。若T℃时,若起始时X为1.20mol,Y为1.00mol,则平衡时Y的转化率为80% |
| B.图②中曲线表示向弱酸HA的稀溶液中加水稀释 |
| C.图③b曲线表示反应CH2=CH2(g)+H2(g)→CH3-CH3(g) △H<0,使用催化剂时,反应过程中的能量变化 |
| D.图④表示向NH4Al(SO4)2溶液中滴加过量的NaOH溶液 |
对可逆反应N2(g)+3H2(g) 2NH3(g),△H=-92.4 kJ.mol-1下列叙
2NH3(g),△H=-92.4 kJ.mol-1下列叙
述正确的是
| A.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大 |
| B.若单位时间内消耗x mol N2,同时生成2x mol NH3,则反应达到平衡状态 |
| C.若达到平衡时,共放出46.2kJ热量,则有l mo1NH3(g)生成 |
| D.达到平衡后,将容器体积减小为原来的一半,重新达到平衡后,c(NH3)变为原平衡时的2倍 |