题目内容
在2L密闭容器中,保持恒温,加热KClO3和MnO2固体混合物制取O2,5min后,生成O232克,则此反应的平均速率可表示为( )
| A.v(O2)=3.2g·L-1·min-1 | B.v(O2)=0.1 mol·L-1·min-1 |
| C.v(KCl)=0.1 mol·L-1·min-1 | D.v(KClO3)=0.0667 mol·L-1·min-1 |
B
解析试题分析:2KClO3 2KCl+3O2↑,由于KClO3、KCl都是固体,浓度不变,所以应该用氧气来表示化学反应速率。V(O2)=Δc÷Δt=(1mol÷2L)÷5min=0.1 mol/( L·min)。因此正确选项为B。
2KCl+3O2↑,由于KClO3、KCl都是固体,浓度不变,所以应该用氧气来表示化学反应速率。V(O2)=Δc÷Δt=(1mol÷2L)÷5min=0.1 mol/( L·min)。因此正确选项为B。
考点:考查化学反应速率的表示的知识。

T ℃时,将6 mol CO2和8 mol H2充入2 L密闭容器中,发生反应CO2(g)+3H2(g)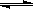 CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是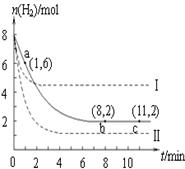
| A.反应开始至a点时v(H2)=1 mol·L-1·min-1 |
| B.若曲线Ⅰ对应的条件改变是升温,则该反应?H>0 |
| C.曲线Ⅱ对应的条件改变是降低压强 |
| D.T ℃时,该反应的化学平衡常数为0.125 |
据报道,美国已经找到名为Trans的铁系催化剂,使氮气和氢气能在常温常压下合成氨。该催化剂的作用是
| A.降低生产能耗 | B.使反应物的化学键不需破坏 |
| C.使反应更完全 | D.使反应放出更多的热量 |
将几滴KSCN(SCN-是“类卤离子”,与氯离子性质相似)溶液加入酸性的含有Fe3+的溶液中,溶液变成血红色。将该红色溶液分为两份,①一份中加入适量KMnO4溶液,红色褪去;②向另一份中通入SO2,红色也褪去。
下列说法不正确的是
| A.①红色褪去的原因可能是KMnO4将SCN-氧化,使[Fe(SCN)]2+消失 |
| B.[Fe(SCN)]2+中Fe3+与SCN-以配位键结合。 |
| C.②红色褪去的原因是SO2具有漂白性 |
| D.SCN-在适当条件下可失去电子被氧化剂氧化为(SCN)2 |
下列措施对增大反应速率明显有效的是
| A.在K2SO4与BaCl2两溶液反应时,增大压强 |
| B.Fe与稀硫酸反应制取H2时,改用浓硫酸 |
| C.Na与水反应时增大水的用量 |
| D.Al在氧气中燃烧生成A12O3,将Al片改成Al粉 |
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)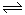 2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4kJ/mol,实验测得起始、平衡时的有关数据如下表: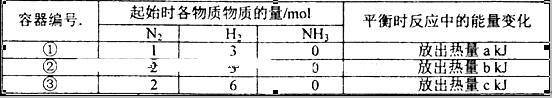
下列叙述正确的是
| A.放出热量关系:a<b <92.4 |
| B.三个容器内反应的平衡常数:③>①>② |
| C.达平衡时氨气的体积分数:①>③ |
| D.N2的转化率:②>①>③ |
4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10 L密闭容器中进行,10s后,水蒸气的物质的量增加了0.60 mol,则此反应的平均速率υ(X)(反应物的消耗速率或产物的生成速率)可表示为
4NO(g)+6H2O(g)在10 L密闭容器中进行,10s后,水蒸气的物质的量增加了0.60 mol,则此反应的平均速率υ(X)(反应物的消耗速率或产物的生成速率)可表示为
| A.υ(NH3)=0.0060 mol/(L·s) |
| B.υ(NO)=0.0040 mol/(L·s) |
| C.υ(O2)=0.0060 mol/(L·s) |
| D.υ(H2O)=0.036 mol/(L·min) |
把4mol A和2.5mol B混合于2L密闭容器中,发生反应:3A(g)+2B(s)  xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol?L-1?min-1 ,下列结论错误的是( )
xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol?L-1?min-1 ,下列结论错误的是( )
| A.A的平均反应速率为0.15 mol?L-1?min-1 |
| B.平衡时,C的浓度为0.25mol?L-1 |
| C.B的平均反应速率为0.1 mol?L-1?min-1 |
| D.平衡时,容器内压强为原来的0.875倍 |
 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是 ( )
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是 ( )