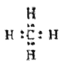题目内容
【题目】请用C、H、O、N、S五种元素回答下列问题
(1)除H外,其它四种元素中,第一电离能最大的元素基态原子电子排布图为______________,电负性最大的元素基态原子核外电子运动状态共有_________种。
(2)五种元素中,由其中两种元素构成甲、乙、丙、丁四种分子,所含原子的数目依次为3、4、6、8,都含有18个电子。甲和乙的主要物理性质比较如下:
熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
甲 | 187 | 202 | 2.6 |
乙 | 272 | 423 | 以任意比互溶 |
①1mol乙分子含有_________个σ键;
②丁分子的中心原子采取_________杂化方式;甲分子的VSEPR模型为_________,丙分子为_________(“极性”或“非极性”)分子。
【答案】![]() 8 3NA sp3 四面体 极性
8 3NA sp3 四面体 极性
【解析】
(1)同一周期,从左到右,元素的第一电离能逐渐增大,但第IIA族、第VA族元素的第一电离能大于相邻元素,同一主族,从上到下,元素的第一电离能减小;元素的非金属性越强,电负性数值越大,据此分析出符合条件的2种元素再解答;
(2)五种元素中,由其中两种元素构成甲、乙、丙、丁四种分子,所含原子的数目依次为3、4、6、8,都含有18个电子,则甲、乙、丙、丁分别是H2S、H2O2、N2H4、C2H6,据此分析解答。
(1)同一周期,从左到右,元素的第一电离能逐渐增大,但第IIA族、第VA族元素的第一电离能大于相邻元素,同一主族,从上到下,元素的第一电离能减小,除H外,其它四种元素中,第一电离能最大的元素是N元素,N元素基态原子核外有7个电子,分别位于1s、2s、2p轨道,该基态原子核外电子排布图为![]() ;元素的非金属性越强,电负性数值越大,电负性最大的元素是O元素,元素的原子核外有几个电子,其基态原子核外电子运动状态就有几种,O原子核外有8个电子,则O原子核外电子有8种运动状态,故答案为:
;元素的非金属性越强,电负性数值越大,电负性最大的元素是O元素,元素的原子核外有几个电子,其基态原子核外电子运动状态就有几种,O原子核外有8个电子,则O原子核外电子有8种运动状态,故答案为:![]() ;8;
;8;
(2)五种元素中,由其中两种元素构成甲、乙、丙、丁四种分子,所含原子的数目依次为3、4、6、8,都含有18个电子,其中甲在水中的溶解度不大,乙易溶于水,二者熔沸点均较低,固态时构成分子晶体,则甲、乙、丙、丁分别是H2S、H2O2、N2H4、C2H6。
①乙分子的结构式为H-O-O-H,共价单键为σ键,每个双氧水分子中含有3个σ键,则1mol双氧水中含有3NAσ键,故答案为:3NA;
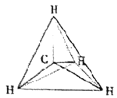
②丁的结构简式为CH3CH3,丁分子的中心原子C原子价层电子对个数是4,且不含孤电子对,C原子杂化方式为sp3杂化;甲分子为H2S,分子中S原子价层电子对个数=2+![]() =,VSEPR模型为四面体结构;丙分子为N2H4,分子中正负电荷重心不重合,为极性分子,故答案为:sp3;四面体;极性。
=,VSEPR模型为四面体结构;丙分子为N2H4,分子中正负电荷重心不重合,为极性分子,故答案为:sp3;四面体;极性。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】下列实验内容能达到实验目的的是
实验目的 | 实验内容 | |
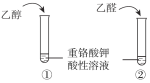
A | 鉴别乙醇与乙醛 |
|
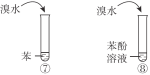
B | 比较乙酸、碳酸、苯酚的酸性 |
|
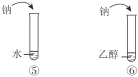
C | 说明烃基对羟基上氢原子活性的影响 | |
D | 说明苯环对取代基上氢原子活性的影响 |
|
A. AB. BC. CD. D