题目内容
【题目】在标准状况下,有一刚性密闭容器,被一可以自由滑动的活塞分成两个密闭的反应器。左侧充入等物质的量的氢气和氧气,右侧充入一氧化碳和氧气的混合气体。同时引燃左右两侧的混合气,反应后恢复到标准状况。反应前后活塞位置如下图所示。则右侧混合气体中一氧化碳和氧气的物质的量之比是____________或___________。(液态水的体积忽略不计)

【答案】1:1;3:1
【解析】
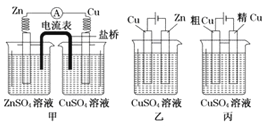
试题分析:假设氢气和氧气的物质的量分别为1mol,开始时左右两侧气体的体积相等,则物质的量之和相等,右侧气体共为2mol,同时引燃左右两侧的混合气,发生反应分别为,左侧:2H2+O2![]() 2H2O,右侧:2CO+O2
2H2O,右侧:2CO+O2![]() 2CO2,左侧剩余气体为0.5molO2,由图可知反应后左右两侧气体的物质的量之比为1:3,则右侧气体的物质的量为1.5mol,当CO过量时,设O2为xmol,则CO为(2-x)mol:
2CO2,左侧剩余气体为0.5molO2,由图可知反应后左右两侧气体的物质的量之比为1:3,则右侧气体的物质的量为1.5mol,当CO过量时,设O2为xmol,则CO为(2-x)mol:
2CO+O2![]() 2CO2
2CO2
2 1 1
2x x 2x
2-x-2x+2x=1.5,x=0.5,所以:n(CO)=1.5mol,n(O2)=0.5mol,n(CO):n(O2)=3:1;
当O2过量时,设CO为ymol,则O2为(2-y)mol,
2CO+O2![]() 2CO2
2CO2
2 1 1
y ![]() y
y
2-y-![]() +y=1.5,y=1,所以:n(CO)=1mol,n(O2)=1mol,n(CO):n(O2)=1:1,故答案为:1:1或3:1。
+y=1.5,y=1,所以:n(CO)=1mol,n(O2)=1mol,n(CO):n(O2)=1:1,故答案为:1:1或3:1。

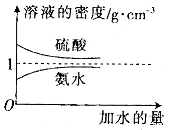
【题目】已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中的信息,回答下列问题 :
溶质的物质的量浓度/ | 溶液的密度/ |
| |
硫酸 |
|
| |
氨水 |
|
|
(1)表中硫酸的质量分数为__________(不写单位,用含![]() 、
、![]() 的代数式表示)。
的代数式表示)。
(2)物质的量浓度为![]()
![]() 的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为___________
的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为___________![]() 。
。
(3)物质的量浓度为![]()
![]() 的氨水与
的氨水与![]()
![]()
![]() 的氨水等质量混合,所得溶液的密度______(填
的氨水等质量混合,所得溶液的密度______(填
“大于”、“小于”或“等于”,下同) ![]()
![]() ,所得溶液的物质的量浓度________
,所得溶液的物质的量浓度________![]()
![]()
![]()
(设混合后溶液的体积变化忽略不计)
(4)若将稀硫酸与氨水混合,写出其反应的离子方程式___________________________.