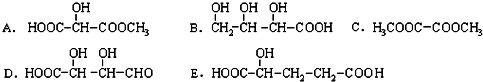题目内容
1.氯气跟碘在加热条件下,以等物质的量进行反应,可得到一种红棕色液体ICl.ICl有很强的氧化性,ICl跟Zn、H2O反应的化学方程式为:2ICl+2Zn=ZnCl2+ZnI2、ICl+H2O=HCl+HIO,下列叙述中正确的是( )| A. | ZnCl2既是氧化产物,又是还原产物 | |
| B. | ICl跟H2O的反应是自身氧化还原反应 | |
| C. | ZnI2既是氧化产物,又是还原产物 | |
| D. | 在ICl跟H2O的反应中,ICl是氧化剂,H2O是还原剂 |
分析 2ICl+2Zn═ZnCl2+ZnI2中Zn元素的化合价升高,I元素的化合价降低,而ICl+H2O═HCl+HIO中,各元素的化合价不变,以此解答该题.
解答 解:A.反应2ICl+2Zn═ZnCl2+ZnI2中,Zn元素化合价升高,Cl元素化合价不变,ZnCl2为氧化产物,故A错误;
B.ICl+H2O═HCl+HIO中,各元素的化合价不变,不属于氧化还原反应,故B错误;
C.2ICl+2Zn═ZnCl2+ZnI2中Zn元素的化合价升高,I元素的化合价降低,ZnI2既是氧化产物,又是还原产物,故C正确;
D.ICl+H2O═HCl+HIO中,各元素的化合价不变,不属于氧化还原反应,故D错误.
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,明确元素的化合价变化是解答本题的关键,注意ICl中I为+1价,Cl为-1价为解答的关键,题目难度不大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
11.下列元素中,最高正化合价数值最大的是( )
| A. | Na | B. | P | C. | S | D. | C |
12.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 在标准状态下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1mol碳正离子CH5+所含的电子数为11NA | |
| C. | 标准状态下,16g甲烷完全燃烧所消耗的氧气的分子数为2NA | |
| D. | 0.5molC3H8分子中含C-H共价键2NA |
16.原子序数小于10的元素X,其原子最外层中未成对电子数最多,含这种元素的阴离子可能是( )
| A. | XO3- | B. | XO32- | C. | XO42- | D. | XO43- |
6.某CaCl2样品中混有FeCl3、MgCl2、NaCl和Na2CO3中的一种或几种杂质.取11.1g样品溶解,得无色溶液,再加入足量AgNO3溶液,得到29.7g沉淀.则样品中( )
| A. | 一定无Na2CO3,可能有FeCl3 | B. | 一定有MgCl2,一定无NaCl | ||
| C. | 一定有MgCl2,可能有Na2CO3 | D. | 一定有MgCl2,可能有NaCl |
13.下列各组物质中,互为同分异构体的是( )
| A. | CH3-CH2-CH2-CH2-CH3和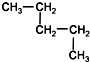 | B. | 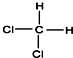 和 和 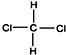 | ||
| C. | CH3-CH3和CH3-CH2-CH3 | D. | 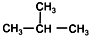 和CH3-CH2-CH2-CH3 和CH3-CH2-CH2-CH3 |
10.有原子序数依次增大的A、B、C、D、E五种短周期元主族素,它们可两两组成甲、乙、丙、丁四种化合物,各化合物中原子个数比关系如下表:
其中A、B两种原子的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多两个;在周期表中,C是E的邻族元素,化学性质活泼;D和E位于同一周期,且D和E的原子序数之和为30.
(1)甲的电子式 ,丁的结构式
,丁的结构式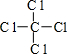
(2)E元素在周期表中的位置是第三周期ⅦA族,其最简单离子的结构示意图为 ,最高价氧化物的水化物化学式为HClO4.
,最高价氧化物的水化物化学式为HClO4.
(3)五种元素中,既可以与盐酸反应,又可以与氢氧化钠溶液反应的是Al(填元素符号),并写出反应的离子方程式:2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑.
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
(1)甲的电子式
 ,丁的结构式
,丁的结构式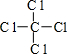
(2)E元素在周期表中的位置是第三周期ⅦA族,其最简单离子的结构示意图为
 ,最高价氧化物的水化物化学式为HClO4.
,最高价氧化物的水化物化学式为HClO4.(3)五种元素中,既可以与盐酸反应,又可以与氢氧化钠溶液反应的是Al(填元素符号),并写出反应的离子方程式:2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑.
11.属于苯的同系物是( )
| A. | 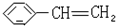 | B. | 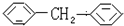 | C. |  | D. | 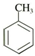 |
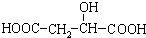 )广泛存在于水果中,尤以苹果、葡萄、西瓜、山
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山