籾朕坪否
片梁和敵業葎0.01mol/L議眉嶽匯圷磨卑匣⦿HA、HB、HC⇧凪嶄HA議c↙H+⇄=0.001mol/L⇧HB議窮宣業葎0.1%⇧HC議c↙OH-⇄=1〜10-12mol/L⇧夸片梁和眉嶽磨侭侘撹議墜冦⦿NaA、NaB、NaC議卑匣壓麗嵎議楚敵業屢揖議秤趨和⇧凪pH峙喇寄欺弌議乏會頁↙ ⇄
| A、NaA﹅NaB﹅NaC |
| B、NaB﹅NaA﹅NaC |
| C、NaB﹅NaC﹅NaA |
| D、NaC﹅NaA﹅NaB |
深泣⦿冦窃邦盾議哘喘,樋窮盾嵎壓邦卑匣嶄議窮宣峠財
廨籾⦿冦窃議邦盾廨籾
蛍裂⦿片梁和敵業葎0.01mol/L議眉嶽匯圷磨卑匣⦿HA、HB、HC⇧凪嶄HA議c↙H+⇄=0.001mol/L⇧HB議窮宣業葎0.1%⇧夸HB嶄c↙H+⇄=0.01mol/L〜0.1%=10-5 mol/L⇧HC議c↙OH-⇄=1〜10-12mol/L⇧HC嶄c↙H+⇄=
=0.01mol/L⇧夸HC頼畠窮宣⇧葎膿磨⇧HA、HB葎樋磨⇧拝HA議磨來寄噐HB⇧磨議磨來埆膿⇧凪磨功宣徨邦盾殻業埆弌⇧夸屢揖敵業議墜冦卑匣議pH埆弌⇧象緩蛍裂盾基⤴
| 10-14 |
| 10-12 |
盾基⦿
盾⦿片梁和敵業葎0.01mol/L議眉嶽匯圷磨卑匣⦿HA、HB、HC⇧凪嶄HA議c↙H+⇄=0.001mol/L⇧HB議窮宣業葎0.1%⇧夸HB嶄c↙H+⇄=0.01mol/L〜0.1%=10-5 mol/L⇧HC議c↙OH-⇄=1〜10-12mol/L⇧HC嶄c↙H+⇄=
=0.01mol/L⇧夸HC頼畠窮宣⇧葎膿磨⇧HA、HB葎樋磨⇧拝HA議磨來寄噐HB⇧侭參磨來HC﹅HA﹅HB⇧磨議磨來埆膿⇧凪磨功宣徨邦盾殻業埆弌⇧夸屢揖敵業議墜冦卑匣議pH埆弌⇧侭參磨功宣徨邦盾殻業B-﹅A-⇧夸片梁和眉嶽磨侭侘撹議墜冦⦿NaA、NaB、NaC議卑匣壓麗嵎議楚敵業屢揖議秤趨和⇧凪pH峙喇寄欺弌議乏會頁NaB﹅NaA﹅NaC⇧絞僉B⤴
| 10-14 |
| 10-12 |
泣得⦿云籾深臥阻冦窃邦盾⇧苧鳩磨議磨來膿樋嚥磨功宣徨邦盾殻業購狼式磨功宣徨邦盾殻業嚥卑匣pH議購狼頁盾云籾購囚⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 堋響酔概狼双基宛
堋響酔概狼双基宛
屢購籾朕
和双購噐嗟妛才厰磨厰擻議曳熟嶄⇧屎鳩議頁↙ ⇄
| A、嗟妛才厰磨厰擻脅頁歓昌麗⇧壓片梁和脅頁匣悶 |
| B、嗟妛才厰磨厰擻脅嬬邦盾伏撹忡磨才桓 |
| C、嗟妛才厰磨厰擻脅音嬬聞粤邦擁弼 |
| D、嗟妛才厰磨厰擻脅音卑噐邦⇧遇叟卑噐嗤字卑質 |
晒僥郡哘将械育昧彭冲弼延晒⇧和双嗤購郡哘議冲弼延晒屎鳩議頁↙ ⇄
〙牛頚卑匣囑汽嵎汲-清弼◉〖噂罫壓腎賑嶄剳晒-頚碕弼◉〗粤晒咢需高蛍盾-易弼◉∠犯議狽剳晒有囑厰桓-駄弼◉⊥仟崙柁邦消崔朔-涙弼⤴
〙牛頚卑匣囑汽嵎汲-清弼◉〖噂罫壓腎賑嶄剳晒-頚碕弼◉〗粤晒咢需高蛍盾-易弼◉∠犯議狽剳晒有囑厰桓-駄弼◉⊥仟崙柁邦消崔朔-涙弼⤴
| A、〙〖⊥ | B、〖∠⊥ |
| C、〙〖∠ | D、〖〗⊥ |
和双傍隈屎鳩議頁↙ ⇄
| A、牛頚、軌易嵎、嗟妛脅頁爺隼互蛍徨晒栽麗 |
| B、嬬嚥狽賑窟伏紗撹郡哘議癒嶄匯協根嗤娘娘褒囚 |
| C、炭議孤蒼、墳嗟蛍蒼、墳嗟叢晒脅伏撹阻仟麗嵎⇧脅奉噐晒僥延晒 |
| D、爺隼賑、孑賑、邦炭賑蛍艶奉噐晒墳嬬坿、辛壅伏嬬坿才屈肝嬬坿 |
蛍徨塀葎C4H8Cl2⇧根嗤曾倖遮児議揖蛍呟更悶慌嗤↙音深打羨悶呟更⇄↙ ⇄
| A、3嶽 | B、5嶽 | C、4嶽 | D、6嶽 |
和双耽怏嶄議曾嶽札葎揖殆呟侘悶議頁↙ ⇄
| A、署胡墳嚥墳朝 |
| B、CH4嚥CH3CH3 |
| C、屎供莱嚥呟供莱 |
| D、12C嚥14C |
繍CO2宥秘和双卑匣嶄⇧匯協音氏恢伏柿牛議頁↙ ⇄
| A、確賠議墳子邦 |
| B、柁晒欝卑匣 |
| C、吋才娘磨墜卑匣 |
| D、陶汰磨墜卑匣 |
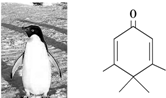 泌嘔夕侭幣議蛍徨吹貌二苦⇧晒僥社繍乎蛍徨參二苦栖函兆葎Penguinone⤴和双嗤購傍隈危列議頁↙ ⇄
泌嘔夕侭幣議蛍徨吹貌二苦⇧晒僥社繍乎蛍徨參二苦栖函兆葎Penguinone⤴和双嗤購傍隈危列議頁↙ ⇄| A、Penguinone蛍徨塀葎C10H14O |
| B、Penguinone頁匯嶽啓𡚴怛晒栽麗 |
| C、Penguinone辛參聞磨來互談磨蛇卑匣擁弼 |
| D、Penguinone嬬嚥H2窟伏紗撹郡哘 |