题目内容
下列说法正确的是( )
| A、淀粉、蛋白质、油脂都是天然高分子化合物 |
| B、能与氢气发生加成反应的烃中一定含有碳碳双键 |
| C、煤的干馏、石油分馏、石油裂化都生成了新物质,都属于化学变化 |
| D、天然气、沼气、水煤气分别属于化石能源、可再生能源和二次能源 |
考点:淀粉的性质和用途,清洁能源,石油的分馏产品和用途,石油的裂化和裂解,有机高分子化合物的结构和性质
专题:有机化学基础
分析:A.相对分子质量在10000以上的有机化合物为高分子化合物;
B.碳碳三键能与氢气发生加成反应;
C.化学变化一定有新物质的生成;
D.天然气是由古代生物在地下发生复杂的变化形成的,沼气是由植物秸秆发酵形成的,水煤气是由C与水蒸气反应生成的.
B.碳碳三键能与氢气发生加成反应;
C.化学变化一定有新物质的生成;
D.天然气是由古代生物在地下发生复杂的变化形成的,沼气是由植物秸秆发酵形成的,水煤气是由C与水蒸气反应生成的.
解答:
解:A.油脂相对分子质量较小,不属于高分子化合物,故A错误;
B.能与氢气发生加成反应的烃中可能含有碳碳双键,也可能含有碳碳三键,故B错误;
C.石油分馏是利用物质的沸点不同而分离物质的方法,没有新物质的生成属于物理变化,故C错案;
D.天然气、沼气、水煤气分别属于化石能源、可再生能源和二次能源,故D正确;
故选:D.
B.能与氢气发生加成反应的烃中可能含有碳碳双键,也可能含有碳碳三键,故B错误;
C.石油分馏是利用物质的沸点不同而分离物质的方法,没有新物质的生成属于物理变化,故C错案;
D.天然气、沼气、水煤气分别属于化石能源、可再生能源和二次能源,故D正确;
故选:D.
点评:本题侧重考查有机物基础知识的考查,题目难度不大,注意化学变化与物理变化的实质是:有新物质是生成.

练习册系列答案
相关题目
反应A(g)+2B(g)═C(g)的反应过程中能量变化如图所示.下列相关说法正确的是( )


| A、该反应是吸热反应 |
| B、催化剂改变了该反应的焓变 |
| C、曲线b表示使用催化剂后的能量变化 |
| D、该反应的焓变△H=-510kJ?mol-1 |
下列说法正确的是( )
| A、0.1 mol/L的下列溶液:①NH4Al(SO4)2 ②NH4Cl ③NH3?H2O ④CH3COONH4中c(NH4+)由大到小的顺序是:②>①>④>③ |
| B、NaHCO3溶液和Na2CO3溶液混合一定存在:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| C、25℃时,pH=11的氨水和pH=3的硫酸等体积混合:c(NH4+)>c(SO42-)>c(OH-)>c(H+) |
| D、室温下,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液至中性,混合溶液中各离子浓度大小关系:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
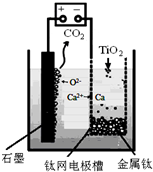 研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中,不正确的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中,不正确的是( )| A、由TiO2制得1mol金属Ti,理论上外电路转移4mol电子 |
| B、阳极的电极反应式为:C+2O2--4e-═CO2↑ |
| C、若用铅蓄电池作该装置的供电电源,“+”接线柱应连接Pb电极 |
| D、在制备金属钛前后,整套装置中CaO的总量不变 |
室温下浓度为0.01mol/L的三种一元酸溶液:HA、HB、HC,其中HA的c(H+)=0.001mol/L,HB的电离度为0.1%,HC的c(OH-)=1×10-12mol/L,则室温下三种酸所形成的钠盐:NaA、NaB、NaC的溶液在物质的量浓度相同的情况下,其pH值由大到小的顺序是( )
| A、NaA>NaB>NaC |
| B、NaB>NaA>NaC |
| C、NaB>NaC>NaA |
| D、NaC>NaA>NaB |
 科研、生产中常涉及钠、硫及其化合物.如图为钠硫高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS═Na2Sx,下列叙述错误的是( )
科研、生产中常涉及钠、硫及其化合物.如图为钠硫高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS═Na2Sx,下列叙述错误的是( )| A、该电池的负极材料是钠 |
| B、陶瓷材料的作用是导电(电解质)兼隔膜 |
| C、当电池中转移1.204×1024个电子时,消耗钠的物质的量为2mol |
| D、外电路中电子的移动方向是:S→Na |
已知某非金属元素R的气态氢化物的分子式为RHm,它的最高价氧化物对应的水化物的分子中有b个氧原子,则这种酸的分子式为( )
| A、H2b-8+mROb |
| B、H2b-8-mROb |
| C、H8-m-2bROb |
| D、Hm+8+2bROb |
下列物质的水溶液中,除水分子外,不存在其他分子的是( )
| A、H3PO4 |
| B、NaF |
| C、HNO3 |
| D、KHS |
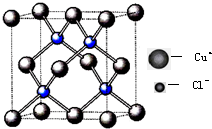 利用反应:Cu2Cl2+C2H2+2NH3→Cu2C2(乙炔亚铜,红色)+2NH4Cl可检验乙炔.
利用反应:Cu2Cl2+C2H2+2NH3→Cu2C2(乙炔亚铜,红色)+2NH4Cl可检验乙炔.