题目内容
【题目】请根据要求填空:
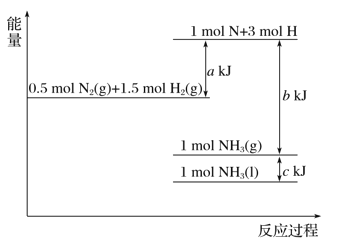
(1)化学反应过程中,不仅有物质的变化,还伴随有能量的变化。根据下图写出反应的热化学方程式:_________________________________。

(2)化学反应速率和化学平衡是化学反应原理的重要组成部分。
将4.0mol PCl3和2.0 mol Cl2充入10 L恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g)![]() PCl5(g),经2 min达到平衡时,PCl5为0.40 mol。
PCl5(g),经2 min达到平衡时,PCl5为0.40 mol。
①在0~2 min 内,用Cl2 表示的反应速率为:v(Cl2)=_____ mol·L-l·min-1;
②达到平衡时,PCl3的转化率为___________________。
③如果再通入1.0 mol Cl2,相同温度下重新达到平衡时,PCl5的物质的量________________。(填标号)
A.增大 B.减小 C.不变
【答案】 CO(g)+H2O(g)==CO2(g)+H2(g) ΔH=-41kJ·mol-1 0.02 10% A
【解析】试题分析(1)根据图示,1molCO2(g)与1mol H2(g)反应,生成1mol CO(g)和 1mol H2O(g)放出41 kJ的能量;(2)利用“三段式”计算。
解析:根据图示,1molCO2(g)与1mol H2(g)反应,生成1mol CO(g)和 1mol H2O(g)放出41 kJ的能量,该反应热化学方程式是CO(g)+H2O(g)==CO2(g)+H2(g) ΔH=-41kJ·mol-1;
(2)

①在0~2min内,用Cl2表示的反应速率为:v(Cl2)= ![]() 0.02 mol·L-l·min-1;②达到平衡时,PCl3的转化率为
0.02 mol·L-l·min-1;②达到平衡时,PCl3的转化率为![]() ;③如果再通入1.0molCl2,平衡正向移动,PCl5的物质的量增大,选A。
;③如果再通入1.0molCl2,平衡正向移动,PCl5的物质的量增大,选A。

 优学名师名题系列答案
优学名师名题系列答案