题目内容
【题目】室温下用![]() 分别滴定
分别滴定![]() 的盐酸和醋酸的曲线如图所示,下列说法正确的是
的盐酸和醋酸的曲线如图所示,下列说法正确的是

A.Ⅰ表示的是滴定盐酸的曲线
B.![]() 时,两份溶液中:
时,两份溶液中:![]()
C.![]() 时,两份溶液中:
时,两份溶液中:![]()
D.![]() 时,醋酸溶液中:
时,醋酸溶液中:![]()
【答案】BC
【解析】
A. 醋酸是弱电解质,HCl是强电解质,相同浓度的醋酸和HCl溶液,醋酸的pH>盐酸的pH,所以I是滴定醋酸的曲线,A项错误;
B. 醋酸钠水解呈碱性,氯化钠不水解,pH=7时,盐酸所用NaOH溶液的体积等于20.00mL,醋酸所用NaOH溶液的体积小于20.00mL,两份溶液中:c(Cl-)>c(CH3COO-),B项正确;
C. V(NaOH)=15.00mL时,根据物料守恒可知:两种溶液中,4c(Na+)=3c(Cl-),4c(Na+)=3c(CH3COOH)+3c(CH3COO-),故c(Cl-)=c(CH3COOH)+c(CH3COO-),C项正确;
D. 当V(NaOH)=10.00mL时,溶液中的溶质为醋酸钠和醋酸的(1:1)混合液,溶液显酸性;根据电荷守恒关系:c(OH-)+c(CH3COO-)=c(Na+)+c(H+)可知,当c(H+)>c(OH-),则有 c(CH3COO-)>c(Na+),D项错误;
答案选BC。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g) +Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A.反应前2 min的平均速率v(Z)=2.0×10-3 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
D.该温度下此反应的平衡常数K=1.44
【题目】用50mL0.50mol/L 盐酸与50 mL0.55mol/LNaOH溶液,在右图装置中进行中和热的测定,请回答下列问题:
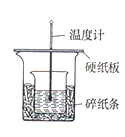
(1)从实验装置看,图中尚缺少的一种玻璃用品是________。
(2)在操作正确的前提下,提高中和热测定准确性的关键是________。
(3)做1次完整的中和热测定实验,温度计需使用________次,某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?________。
(4)某同学实验记录数据如下表所示假设盐酸和氢氧化钠溶液的密度都是1g/mL,又知中和反应后生成溶液的比热容c=4.18J/(g.℃)根据该同学的实验数据计算,该实验测的中和热△H=________。
温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | |||
HCl | NaOH | ||||
1 | 20.0 | 20.1 | 23.2 | ||
2 | 20.2 | 20.4 | 23.4 | ||
3 | 20.5 | 20.6 | 23.6 | ||