题目内容
【题目】已知0.1mol![]() L-1的二元酸H2A溶液的pH=4.0则下列说法中正确的是
L-1的二元酸H2A溶液的pH=4.0则下列说法中正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中有:2c(Na+)=3c(A2-)+3c(HA-)+3c(HA)
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
【答案】B
【解析】
A、在Na2A、NaHA两溶液中,A2-离子水解,HA-存在电离和水解,所以离子种类相同,A错误;
B.根据物料守恒中,在Na2A中存在c(Na+)=2c(A2-)+2c(HA-)+2c(HA),在NaHA中存在c(Na+)=c(A2-)+c(HA-)+c(HA),两种物质的物质的量浓度相等,所以得2c(Na+)=3c(A2-)+3c(HA-)+3c(HA),B正确;
C.根据电荷守恒得c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-),C错误;
D.在Na2A溶液中,A2-离子分步水解,溶液呈碱性;一定有:c(Na+)>c(OH-)>c(A2-)>c(H+),D错误;
选B.

【题目】下列说法正确的是![]()
化学式 | 电离常数 |
|
|
|
|
| |
HF |
|
A.在![]() 酸式盐
酸式盐![]() 溶液中一定存在:
溶液中一定存在:![]()
B.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:![]()
C.已知某温度下常见弱酸的电离平衡常数如上表:相同物质的量浓度的![]() 、NaF、
、NaF、![]() 、
、![]() 水溶液,溶液中离子总数由小到大排列的顺序是
水溶液,溶液中离子总数由小到大排列的顺序是![]()
D.pH均等于3的醋酸与盐酸溶液等体积混合后,溶液的pH基本不变
【题目】外观与氯化钠相似的亚硝酸钠(Na2NO2)在生活中应用十分广泛,如可用作建筑钢材缓蚀剂、肉制品发色剂等。已知:2NO+Na2O2=2NaNO2 2NO2+Na2O2=2NaNO3
I.某学习小组设计如图装置制备亚硝酸钠(夹持装置已省略)
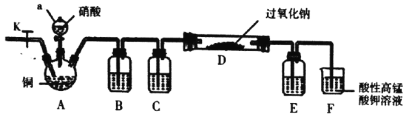
(1)仪器a的名称为________。
(2)装置B、C、E中的试制可选择___。
A 水、浓硫酸、浓硫酸
B 氢氧化钠溶液、浓硫酸、浓硫酸
C 酸性高锰酸钾溶液、浓硫酸、氢氧化钠溶液
D 水、浓硫酸、氢氧化钠溶液
(3)反应开始时先打开止水夹K,通入氮气至F中产生大量气泡,该操作的目的是________。
(4)装置D中的实验现象是________。
(5)装置F中发生反应的离子方程式为________。
Ⅱ.工业上可以用烧碱溶液吸收硝酸厂的尾气制得亚硝酸钠。某学习小组设计如下实验方案测定该产品中亚硝酸钠的质量分数。取1.500g产品配成250mL溶液,取25.00mL溶液于锥形瓶中加入过量的稀硫酸和碘化钾溶液充分反应后,加入适当的指示剂,用0.1000mol/L Na2S2O3标准溶液进行滴定,记录数据如下表。
实验序号 | 1 | 2 | 3 |
Na2S2O3标准溶液体积/mL | 20.02 | 19.98 | 20.00 |
已知: 2NaNO2+2KI+2H2SO4 =2NO↑+I2+2H2O+Na2SO4+K2SO4 2Na2S2O3+I2=Na2S4O6+2NaI
(6)合适的指示剂是________
(7)该产品的纯度为________。
(8)经过讨论,同学认为该产品中可能含有硝酸钠,它会使测定结果________(填“偏高”、“偏低”、“无影响”) 。