题目内容
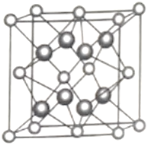
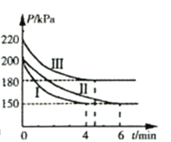
【题目】工业上用CO2和NH3合成尿素 [CO(NH2)2]。某研发小组为合成尿素进行如下实验:向5L恒容密闭容器中通入0.2molNH3和0.1molCO2,分别进行Ⅰ、Ⅱ、Ⅲ三组实验。在不同条件下发生反应:![]() ,反应体系总压强随时间的变化曲线如图所示。
,反应体系总压强随时间的变化曲线如图所示。
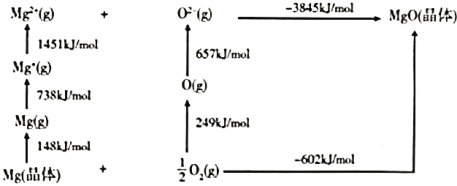
(1)已知:
①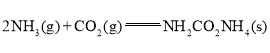
![]()
②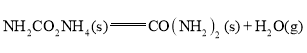
![]()
用CO2和NH3合成尿素的热化学方程式为________。
(2)Ⅰ、Ⅱ、Ⅲ三组实验中,反应温度最高的是________。(填“Ⅰ”、“Ⅱ”或“Ⅲ”)
(3)Ⅰ、Ⅲ两组实验中,NH3转化率较高的是________。(填“Ⅰ”或“Ⅲ”)
(4)若要增加实验Ⅱ的反应速率并提高NH3转化率,改变下列条件可以实现的是________(填标号)
A.增加CO2的物质的量 B.加入惰性气体使压强增大
C.升高反应的温度 D.改用2L的容器进行实验
(5)Ⅰ、Ⅱ两组实验中,反应达到平衡的时间不同,可能的原因是________。
(6)第Ⅱ组实验开始6min内NH3的平均反应速率为________![]() ,平衡常数
,平衡常数![]() ________。
________。
【答案】![]()
![]() Ⅲ Ⅰ AD 使用了不同的催化剂 0.0025 960
Ⅲ Ⅰ AD 使用了不同的催化剂 0.0025 960
【解析】
(1)根据盖斯定律进行计算;
(2)在相同的容器的反应器中,投入相同物质的量的反应物,但是反应开始的时候,Ⅲ中的压强最高,而Ⅰ和Ⅱ的压强相同,在物质的量、体积相同的情况下,压强和温度成正比;可知Ⅰ和Ⅱ的反应温度相同,反应Ⅲ的温度较Ⅰ和Ⅱ高;
(3)该反应是放热反应,升高温度,平衡逆向移动,NH3的转化率降低,据此规律进行分析;
(4)A.增加CO2的物质的量,速率加快,NH3的转化率增加;
B.加入惰性气体,但是各物质的浓度不变,不影响反应速率和转化率;
C.升高反应的温度,速率加快,平衡逆向移动;
D.改用2L的容器进行实验,相当于压缩气体,各物质的浓度增大,速率加快,平衡正向移动;
(5)反应Ⅰ和Ⅱ中NH3的转化率相同,但是反应Ⅰ的反应速率更快,说明反应Ⅰ和Ⅱ使用了不同的催化剂;
(6)在体积不变的情况下,压强和物质的量成正比。反应开始时,0.2molNH3和0.1molCO2对应的压强为200kPa,达到平衡时,压强为150KPa,可得达到平衡时,气体的总物质的量![]() ,假设CO2反应了xmol,根据反应列三等式,计算出x,从而计算出6min内NH3的平均反应速率,反应的平衡常数。
,假设CO2反应了xmol,根据反应列三等式,计算出x,从而计算出6min内NH3的平均反应速率,反应的平衡常数。
(1)根据盖斯定律,反应①+反应②可得目标反应,CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g),△H=△H1+△H2==(-159.5+116.5)kJ·mol-1=-43kJ·mol-1;
CO(NH2)2(s)+H2O(g),△H=△H1+△H2==(-159.5+116.5)kJ·mol-1=-43kJ·mol-1;
答案为CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g)△H=-43kJ·mol-1;
CO(NH2)2(s)+H2O(g)△H=-43kJ·mol-1;
(2)在相同的容器的反应器中,投入相同物质的量的反应物,但是反应开始的时候,Ⅲ中的压强最高,而Ⅰ和Ⅱ的压强相同,在物质的量、体积相同的情况下,压强和温度成正比;可知Ⅰ和Ⅱ的反应温度相同,反应Ⅲ的温度较Ⅰ和Ⅱ高;所以Ⅰ、Ⅱ、Ⅲ三组实验中,温度最高的是Ⅲ;
(3)该反应是放热反应,升高温度,平衡逆向移动,NH3的转化率降低;实验Ⅰ的温度低,可知实验Ⅰ中NH3的转化率较高;
(4)A.增加CO2的物质的量,生成物浓度增加,化学反应速率增加,NH3的转化率也增加,A符合题意;
B.加入惰性气体,但是各物质的浓度不变,反应速率和NH3的转化率均不变,B不符合题意;
C.升高反应的温度,化学反应速率增加,但是平衡逆向移动,NH3的转化率降低,C不符合题意;
D.改用2L的容器进行实验,相当于压缩气体,各物质的浓度增大,反应速率增加;压缩体积,平衡正向移动,NH3的转化率增加,D符合题意;
答案选AD;
(5)反应Ⅰ和Ⅱ中NH3的转化率相同,但是反应Ⅰ的反应速率更快,说明反应Ⅰ和Ⅱ使用了不同的催化剂;
(6)在体积不变的情况下,压强和物质的量成正比。反应开始时,0.2molNH3和0.1molCO2对应的压强为200kPa,达到平衡时,压强为150KPa,可得达到平衡时,气体的总物质的量![]() ,假设CO2反应了xmol,根据三等式,有;
,假设CO2反应了xmol,根据三等式,有;

则有0.2-2x+0.1-x+x=![]() ,得x=
,得x=![]() ,6min内NH3的平均反应速率
,6min内NH3的平均反应速率 ;平衡常数
;平衡常数 。
。

【题目】下列实验现象描述正确的是( )
选项 | 实 验 | 现 象 |
A | 向氢氧化钠溶液中滴加FeCl3饱和溶液 | 有氢氧化铁胶体产生 |
B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝滴落下来 |
C | 向滴有酚酞的溶液中加入足量Na2O2粉末 | 溶液变红 |
D | 加热放在坩埚中的小块钠 | 钠先熔化成光亮 |
A.AB.BC.CD.D
【题目】随着新能源汽车产业的快速发展,带来大量的废旧电池,一种以废旧磷酸铁锂电池正极为原料回收铝、铁和锂元素的工艺流程如下:
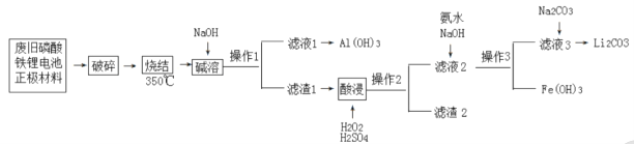
已知:①![]() 易溶于硫酸中。
易溶于硫酸中。
②磷酸铁锂电池正极材料:磷酸铁锂![]() ,乙炔黑(主要成分碳单质,着火点大于750℃)导电剂和有机粘结剂PVDF(一种高分子有机物),均匀混合后涂覆于铝箔上。
,乙炔黑(主要成分碳单质,着火点大于750℃)导电剂和有机粘结剂PVDF(一种高分子有机物),均匀混合后涂覆于铝箔上。
回答下列问题:
(1)破碎的作用是________,烧结的主要目的是________。
(2)碱溶发生的非氧化还原反应的离子方程式是________________。
(3)若在实验室中进行操作1、2、3,需要用到的玻璃仪器有________。
(4)滤渣1酸浸的目的是________。
(5)滤渣2主要成分是________。
(6)pH与Fe、Li沉淀率关系如下表,为使滤液2中Fe、Li分离,溶液的pH应调节为________。
溶液pH与Fe、Li沉淀率关系
pH | 3.5 | 5 | 6.5 | 8 | 10 | 12 |
Fe沉淀率 | 66.5 | 79.2 | 88.5 | 97.2 | 97.4 | 98.1 |
Li沉淀率 | 0.9 | 1.3 | 1.9 | 2.4 | 4.5 | 8.0 |
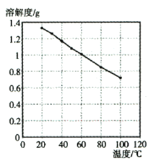
(7)碳酸锂的溶解度随温度变化如下图所示。向滤液3中加入![]() ,将温度升至90℃是为了提高沉淀反应速率和________。
,将温度升至90℃是为了提高沉淀反应速率和________。