题目内容
17.23Na与23Na+比较,相同的是( )| A. | 微粒半径 | B. | 化学性质 | C. | 最外层电子数 | D. | 中子数 |
分析 23Na失去一个电子得到23Na+,根据钠原子和钠离子的结构来分析稳定性和化学性质.
解答 解:A、23Na+是钠原子失去一个电子后形成的,电子层数减少一层,则Na的半径大于23Na+的半径,所以二者的半径不同,故A错误;
B、因23Na+是钠原子失去一个电子后形成的最外层有8个电子的稳定结构,而钠原子最外层有1个电子,容易失去1个电子,所以它们的化学性质不同,故B错误;
C、23Na+是钠原子失去一个电子后形成的最外层有8个电子的稳定结构,而钠原子最外层有1个电子,所以二者最外层电子数不同,故C错误;
D、23Na+是钠原子失去一个电子后形成的,中子数没有改变,所以具有相同的中子数数,故D正确.
故选D.
点评 本题考查原子和离子的转化及它们的性质的分析,学生应能从微粒的结构的角度来分析,明确最外层8电子是稳定结构来分析性质,题目难度不大

练习册系列答案
相关题目
8.据某科学杂志报道,国外发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60结构.下列叙述不正确的是( )
| A. | 该物质的熔点不会很高、硬度不会很大 | |
| B. | 该物质形成的晶体属于分子晶体 | |
| C. | 该物质分子中Si60被包裹在C60里面 | |
| D. | 该物质的相对分子质量为2400 |
5.下列关于铵盐的叙述中正确的是( )
| A. | 都是离子化合物 | B. | 受热都能分解出氨气 | ||
| C. | 都易溶于水 | D. | 都可以与碱反应放出氨气 |
12.关于下列各图的叙述正确的是( )
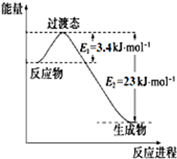
| A. | 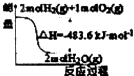 表示H2与O2发生反应过程中的能量变化,则H2的标准燃烧热为△H=-483.6kJ•mol-1 | |
| B. | 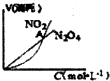 表示恒温恒容条件下发生的可逆反应2NO2?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 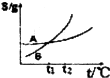 表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A | |
| D. | 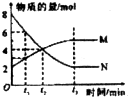 图中在t2时刻正反应速率大于逆反应速率 |
9.下列各组元素性质或原子结构递变情况错误的是( )
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正化合价依次增大 | |
| C. | N、O、F原子半径依次增大 | |
| D. | Na、K、Rb的电子层数依次增多 |
6.能鉴别CO2和SO2的试剂是( )
| A. | 紫色石蕊试液 | B. | 氯化钡溶液 | ||
| C. | 酸性高锰酸钾溶液 | D. | 澄清石灰水 |

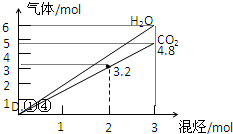 两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,
两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,