题目内容
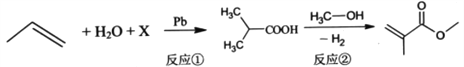
【题目】二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺. 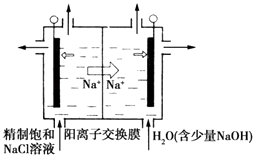
(1)①如图装置用石墨作电极,在一定条件下电解饱和食盐水制取ClO2 . 写出阳极产生ClO2的电极反应式: . ②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为mol.
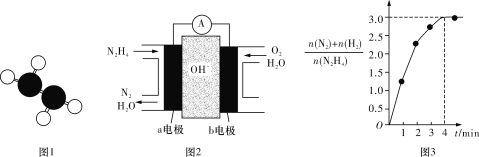
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2﹣离子.电池工作时正极反应为 .
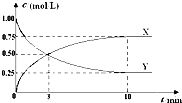
(3)若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液.
离子 | Cu2+ | H+ | Cl﹣ | SO42﹣ |
c/molL﹣1 | 1 | 4 | 4 | 1 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的物质的量为mol.
【答案】
(1)Cl﹣﹣5e﹣+2H2O=ClO2↑+4H+;0.01
(2)O2+4e﹣=2O2﹣
(3)0.1
【解析】解:(1)①阳极发生氧化反应,由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,结合电荷守恒可知,同时生成氢离子,阳极电极反应式为:Cl﹣﹣5e﹣+2H2O=ClO2↑+4H+,
所以答案是:Cl﹣﹣5e﹣+2H2O=ClO2↑+4H+;
②在阴极发生2H++2e﹣=H2↑,氢气的物质的量为 ![]() =0.005mol,通过阳离子交换膜的阳离子为+1价离子,故交换膜的阳离子的物质的量为0.005mol×2=0.01mol,所以答案是:0.01;(2)燃料电池,电池的一个电极通 入空气,另一个电极通入甲醇气体,电解质是掺入了 Y2O3的ZrO2晶体,在高温下它能传导O2﹣离子,根据原电池原理,正极O2得到电子生成负极O2﹣:O2+4e﹣=2O2﹣,所以答案是:O2+4e﹣=2O2﹣;(3)电解一段时间后,当两极收集到相同体积(相词条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),100ml溶液中含有c(Cu2+)=1mol/L,c(H+)=4mol/L,c(Cl﹣)=4mol/L,c(SO42﹣)=1mol/L;
=0.005mol,通过阳离子交换膜的阳离子为+1价离子,故交换膜的阳离子的物质的量为0.005mol×2=0.01mol,所以答案是:0.01;(2)燃料电池,电池的一个电极通 入空气,另一个电极通入甲醇气体,电解质是掺入了 Y2O3的ZrO2晶体,在高温下它能传导O2﹣离子,根据原电池原理,正极O2得到电子生成负极O2﹣:O2+4e﹣=2O2﹣,所以答案是:O2+4e﹣=2O2﹣;(3)电解一段时间后,当两极收集到相同体积(相词条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),100ml溶液中含有c(Cu2+)=1mol/L,c(H+)=4mol/L,c(Cl﹣)=4mol/L,c(SO42﹣)=1mol/L;
阳极氯气和阴极氢气相同,设阳极生成的氧气物质的量为x,阴极上也应生成氢气物质的量x
阳极电极反应为:
2Cl﹣﹣ | 2e﹣= | Cl2↑,4OH﹣﹣ | 4e﹣=2H2O+ | O2↑ |
0.4mol | 0.4mol | 0.2mol | 4x | x |
阴极电极反应为:
Cu2++ | 2e﹣= | Cu, |
0.1mol | 0.2mol | 0.1mol |
2H++ | 2e﹣= | H2↑; | 2H++ | 2e﹣= | H2↑ |
0.4mol | 0.4mol | 0.2mol | 2x | x |
依据电子守恒0.4+4x=0.2+0.4+2x
x=0.1mol
阳极上收集到氧气的物质的量0.1mol;
所以答案是:0.1.

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案