题目内容
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子各不相同,分别含有五种阳离子Na+、Mg2+、Al3+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的各一种.
(1)某同学通过比较分析,认为无需检验就可判断其中必有:
A(碳酸盐) 和B(强碱) .(填化学式)
(2)将Cu投入装有C溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.则Cu溶解反应的离子方程式为 .
(3)已知化合物D中含有X,D溶液呈黄色,当D与B的溶液混合时,产生有色沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解.则X为 (填字母).
A.SO32- B.SO42- C.CH3COO- D.SCN-
(4)利用上述已经确定的物质,可以检验出C、E中的阳离子.请简述实验操作步骤、现象及结论 .
(1)某同学通过比较分析,认为无需检验就可判断其中必有:
A(碳酸盐)
(2)将Cu投入装有C溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.则Cu溶解反应的离子方程式为
(3)已知化合物D中含有X,D溶液呈黄色,当D与B的溶液混合时,产生有色沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解.则X为
A.SO32- B.SO42- C.CH3COO- D.SCN-
(4)利用上述已经确定的物质,可以检验出C、E中的阳离子.请简述实验操作步骤、现象及结论
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:(1)根据离子之间结合生成沉淀,不能共存,确定含有的两种物质;
(2)将Cu投入装有C溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,则C中含有NO3-,为硝酸盐;
(3)D中含有X,D溶液呈黄色,则D为含Fe3+,D与B的溶液混合时,产生有色沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解,最后不溶解的沉淀为硫酸钡,则D为Fe2(SO4)3;
(4)C、E中为Al3+、Mg2+,利用氢氧化铝溶于强碱的性质检验.
(2)将Cu投入装有C溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,则C中含有NO3-,为硝酸盐;
(3)D中含有X,D溶液呈黄色,则D为含Fe3+,D与B的溶液混合时,产生有色沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解,最后不溶解的沉淀为硫酸钡,则D为Fe2(SO4)3;
(4)C、E中为Al3+、Mg2+,利用氢氧化铝溶于强碱的性质检验.
解答:
解:(1)因Al3+、Mg2+、Fe3+和OH-反应生成沉淀,Al3+、Mg2+、Ba2+、Fe3+和CO32-反应,则不能共存,所以一定存在的物质为A为Na2CO3和B为Ba(OH)2,
故答案为:Na2CO3;Ba(OH)2;
(2)将Cu投入装有C溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,则C中含有NO3-,Cu溶解反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
(3)D中含有X,D溶液呈黄色,则D为含Fe3+,D与B的溶液混合时,产生有色沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解,最后不溶解的沉淀为硫酸钡,则D为Fe2(SO4)3,则X为SO42-,故答案为:B;
(4)因Al(OH)3能溶于过量Ba(OH)2溶液,检验出C、E中的阳离子的实验操作步骤、现象及结论为往C的溶液中逐渐加入Ba(OH)2溶液直至过量,若先出现白色沉淀后又逐渐溶解,则C中含有Al3+,E中含有Mg2+,若出现白色沉淀而不溶解,则C中含有Mg2+,E中含有Al3+,
故答案为:往C的溶液中逐渐加入Ba(OH)2溶液直至过量,若先出现白色沉淀后又逐渐溶解,则C中含有Al3+,E中含有Mg2+,若出现白色沉淀而不溶解,则C中含有Mg2+,E中含有Al3+.
故答案为:Na2CO3;Ba(OH)2;
(2)将Cu投入装有C溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,则C中含有NO3-,Cu溶解反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
(3)D中含有X,D溶液呈黄色,则D为含Fe3+,D与B的溶液混合时,产生有色沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解,最后不溶解的沉淀为硫酸钡,则D为Fe2(SO4)3,则X为SO42-,故答案为:B;
(4)因Al(OH)3能溶于过量Ba(OH)2溶液,检验出C、E中的阳离子的实验操作步骤、现象及结论为往C的溶液中逐渐加入Ba(OH)2溶液直至过量,若先出现白色沉淀后又逐渐溶解,则C中含有Al3+,E中含有Mg2+,若出现白色沉淀而不溶解,则C中含有Mg2+,E中含有Al3+,
故答案为:往C的溶液中逐渐加入Ba(OH)2溶液直至过量,若先出现白色沉淀后又逐渐溶解,则C中含有Al3+,E中含有Mg2+,若出现白色沉淀而不溶解,则C中含有Mg2+,E中含有Al3+.
点评:本题考查离子推断、实验方案设计等,是对所学知识的综合考查,题目难度较大,综合度较高,旨在考查学生的推断能力与方案设计能力,注意根据反应现象进行推断.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
下列物质中,可以用于制造半导体的是( )
| A、铝 | B、石墨 |
| C、晶体硅 | D、二氧化硅 |
下列说法中正确的是( )
| A、单质硅是将太阳能转化为电能的常用材料 |
| B、能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| C、原子的最外电子层只有1个电子的元素一定是金属元素 |
| D、光束通过稀豆浆,不会产生丁达尔效应 |
下列物质中最简式相同,但既不是同系物,也不是同分异构体的是( )
A、CH3CH=CH2和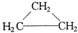 |
| B、乙炔和苯 |
C、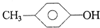 和 和 |
| D、葡萄糖与麦芽糖 |
关于键长、键能和键角,下列说法不正确的是( )
| A、键长大小与两成键原子之间的共用电子对数目有关 |
| B、键角与共价键的方向性有关 |
| C、键能越大,键长越长,共价化合物越稳定 |
| D、键角大小并不决定键长、键能的大小 |