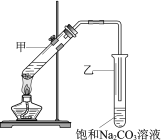
��Ŀ����
����Ŀ��ǰ������Ԫ��A��B��C��D��Eԭ����������������֪��A��Cͬ���壬A��ԭ�������������Ǵ�����3����B���������������ǿ�ᣬ��������ǿ�D��ԭ�Ӱ뾶�ǵ�3��������С�ģ�E���γɹ��������ݵ���ҪԪ�أ���E�����ܺ�ˮ��Ӧ�������з����������
A.A�� B�γɵĻ��������Ϊ�ͻ����
B.A��C���⻯��ķе㣺C>A
C.�����Ӱ뾶��E<D<C
D.E��D�γɵĻ�����ĵ���ʽ��![]()
���𰸡�B
��������
ǰ������Ԫ��A��B��C��D��Eԭ����������������֪��A��Cͬ���壬A��ԭ�������������Ǵ�����3����A��O����C��S��B���������������ǿ�ᣬ��������ǿ�B��Al��D��ԭ�Ӱ뾶�ǵ�����������С�ģ�D��Cl��E���γɹ��������ݵ���ҪԪ�أ���E�����ܺ�ˮ��Ӧ��E��Ca���ݴ˽��
�������Ϸ�����֪A��B��C��D��E�ֱ���O��Al��S��Cl��Ca��
A. A��B�γɵĻ���������������Ϊ�ͻ���ϣ�A��ȷ��
B. ˮ���Ӽ�����������A��C���⻯��ķе㣺C��A��B����
C. ��������Ų���ͬʱ���Ӱ뾶��ԭ���������������С��������Ӱ뾶��E��D��C��C��ȷ��
D. E��D�γɵĻ����������ӻ������Ȼ��ƣ�����ʽΪ![]() ��D��ȷ��
��D��ȷ��
��ѡB��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��[��ѧ����ѡ��3�����ʽṹ������]
��1���������ƳɵĽ���ȼ�ϡ��ǽ�������ȼ�ϡ���������Ӧ�õ��������߿Ƽ�����λ������A��B����ȼ��ʱ���ų������ȣ�������ȼ�ϡ���֪A��BΪ������Ԫ�أ���ԭ�ӵĵ�һ�����ĵ��������±���ʾ��
�����ܣ�KJ/mol�� | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15399 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
��ijͬѧ����������Ϣ���ƶ�B�ĺ�������Ų�����ͼ��ʾ����ͬѧ�����ĵ����Ų�ͼΥ�� ��BԪ��λ�����ڱ���������е� ����
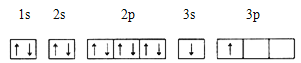
��ACl2������A���ӻ�����Ϊ ��ACl2�Ŀռ乹��Ϊ ��
��2��Feԭ�ӻ�������Χ�н϶���������Ŀչ������һЩ���ӻ������γ�����
�������������ѻ��γɵĽ������У���ԭ�ӵ���λ��Ϊ ��
��д��һ����CN-��Ϊ�ȵ�����ĵ��ʵĵ���ʽ ��
���������������[Fe(CN)6]4-����� ��
A�����ۼ�
B���Ǽ��Լ�
C�����
D������
E������
��3��һ��Al��Fe�Ͻ�����徧������ͼ��ʾ����ݴ˻ش��������⣺
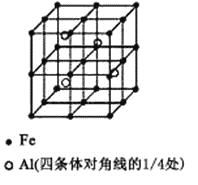
��ȷ���úϽ�Ļ�ѧʽ ��
����������ܶȣ��� g/cm3����˺Ͻ������������Feԭ��֮��ľ���(�ú����Ĵ���ʽ��ʾ�����ػ���)Ϊ cm��