题目内容
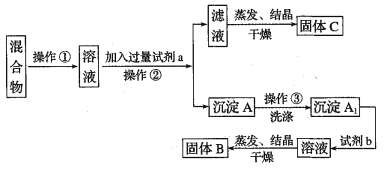
【题目】镧系金属元素铈(Ce)常见有+3、+4两种价态,铈的合金耐高温,可以用来制造喷气推进器零件。铈元素在自然界中主要以氟碳铈矿形式存在,其主要化学成分为CeFCO3。工业上利用氟碳铈矿提取CeCl3的一种工艺流程如下:

(1)为了提高焙烧效率可以采取的措施有______________。(回答两条即可)
(2)假设参与酸浸反应的CeO2和CeF4的物质的量之比为3∶1,试写出相应的化学方程式: ______。有同学认为酸浸过程中用稀硫酸和H2O2替换盐酸更好,其理由是:___________。
(3)常温下,当溶液中的某离子浓度≤1.0×10-5 mol·L-1时,可认为该离子沉淀完全。据此,在生成Ce(OH)3的反应中,加入NaOH溶液至pH至少达到________时,即可视为Ce3+已完全沉淀。{Ksp[Ce(OH)3]=1.0×10-20}。
(4)向Ce(BF4)3中加入KCl溶液,该反应能发生的原因是____________________。
(5)雾霾中含有的污染物NO可以被含Ce4+的溶液吸收,生成NO2-、NO3-,用电解的方法可将上述吸收液中的NO2-转化为稳定的无毒气体,同时将Ce3+再生为Ce4+,其原理如图所示。

①NO2-从电解槽的________(填字母序号)口进入。
②每生成标准状况下11.2 L无毒气体,同时可再生Ce4+________ mol。
【答案】粉碎、逆流、增大空气量 9CeO2+3CeF4+45HCl+3H3BO3=Ce(BF4)3↓+11CeCl3+6Cl2↑+27H2O 不释放氯气,减少对环境的污染 9 KBF4的溶解性比Ce(BF4)3 的溶解性更小 d 3
【解析】
利用氟碳铈矿(主要成分CeFCO3)提取CeCl3的一种工艺流程为,CeFCO3焙烧得CeO2、CeF4,用盐酸和硼酸酸浸,过滤得沉淀Ce(BF)4和CeCl3滤液,Ce(BF)4与氯化钾溶液反应得到CeCl3和KBF4,CeCl3与前面滤液中CeCl3的合并再加氢氧化钠,得Ce(OH)3沉淀,Ce(OH)3沉淀与盐酸反应可得CeCl36H2O,加热CeCl36H2O和NH4Cl的固体混合物可得到无水CeCl3;据此解答。
(1)根据外界条件对反应速率的影响可知为了提高焙烧效率可以采取的措施有粉碎、逆流、增大空气量等。
(2)假设参与酸浸反应的CeO2和CeF4的物质的量之比为3∶1,根据流程可知反应物还有HCl、H3BO3,生成物有Ce(BF4)3沉淀、CeCl3,根据化合价的变化,因元素Ce由+4价变为+3价,化合价降低,由氧化还原反应原理可知,应有元素化合价升高,则应有Cl2生成,结合原子守恒可知相应的化学方程式为9CeO2+3CeF4+45HCl+3H3BO3=Ce(BF4)3↓+11CeCl3+6Cl2↑+27H2O。由于有氯气生成,会污染空气,所以酸浸过程中用稀硫酸和H2O2替换盐酸更好的理由是不释放氯气,减少对环境的污染。
(3)常温下,当溶液中的某离子浓度≤1.0×10-5 mol·L-1时,可认为该离子沉淀完全。根据Ksp[Ce(OH)3]=1.0×10-20可知溶液中氢氧根浓度是![]() =10-5mol/L,因此在生成Ce(OH)3的反应中,加入NaOH溶液至pH至少达到9时,即可视为Ce3+已完全沉淀。
=10-5mol/L,因此在生成Ce(OH)3的反应中,加入NaOH溶液至pH至少达到9时,即可视为Ce3+已完全沉淀。
(4)由于KBF4的溶解性比Ce(BF4)3的溶解性更小,因此向Ce(BF4)3中加入KCl溶液,该反应能发生。
(5)①根据氢离子的移动方向可知左侧电极是阳极,右侧电极是阴极,NO2-得到电子转化为稳定的无毒气体氮气,所以NO2-从电解槽的d口进入。
②每生成标准状况下11.2 L无毒气体,氮气的物质的量是0.5mol,转移0.5mol×6=3.0mol电子,根据电子得失守恒可知同时可再生3.0molCe4+。