题目内容
14. A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:(1)AY2是一种常用的溶剂,为非极性分子(填“极性”或“非极性”),分子中存在2个σ键
(2)X形成的单质与NaOH溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,其晶体与金刚石类似,属于原子晶体.B的最简单氢化物容易液化,理由是分子间形成氢键
(3)X、氧、B元素的电负性由大到小的顺序为O>N>Al(用元素符号作答)
(4)Z的基态原子核外电子排布式为1s22s22p63s23p63d104s1.元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2═ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示不正确的是③(填序号)
①氧化剂是O2②HO2在碱中不能稳定存在
③氧化产物是HO2 ④1mol Z参加反应有1mol电子发生转移
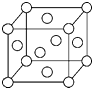
(5)已知Z的晶胞结构如图所示,又知Z的密度为9.00g/cm3,则晶胞边长为$\root{3}{4.72×1{0}^{-23}}$cm
ZYO4常作电镀液,其中YO42-的空间构型是正四面体,Y原子的杂化轨道类型是sp3杂化.
分析 A元素可形成自然界硬度最大的单质,该单质为金刚石,则A为C元素;B与A同周期,核外有三个未成对电子,则B为N元素;根据X原子的第一电离能至第四电离可知,X原子的第四电离能剧增,则X表现+3价,所以X为Al元素;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质,则Y为S元素;Z的一种同位素的质量数为63、中子数为34,则质子数=63-34=29,故Z为Cu元素,据此进行解答.
解答 解:A元素可形成自然界硬度最大的单质,该单质为金刚石,则A为C元素;B与A同周期,核外有三个未成对电子,则B为N元素;根据X原子的第一电离能至第四电离可知,X原子的第四电离能剧增,则X表现+3价,所以X为Al元素;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质,则Y为S元素;Z的一种同位素的质量数为63、中子数为34,则质子数=63-34=29,故Z为Cu元素.
(1)AY2化学式是CS2,其结构式为S=C=S,为直线型结构,属于非极性分子,其分子中每个双键中含有1个σ键,所以CS2分子存在2个σ键,故答案为:非极性;2;
(2)X是Al元素,铝与NaOH溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
XB是CN,晶体与金刚石类似,属于原子晶体;
B的最简单氢化物是NH3,N原子电负性大,分子间形成氢键,所以容易液化,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;原子;分子间形成氢键;
(3)非金属性越强,电负性越强,Al、O、N元素的电负性与非金属性一致,则三种元素电负性大到小顺序为:O>N>Al,故答案为:O>N>Al;
(4)Z为29号Cu元素,根据构造原理,其基态原子核外电子排布式为:1s22s22p63s23p63d104s1;?
①O2中氧元素的化合价是0价,HO2中氧元素的平均化合价是-0.5价,化合价降低作氧化剂,故①正确;?
②HO2为超氧酸,应具有酸性,可与碱反应,故HO2在碱中不能稳定存在,故②正确;
③还原产物是HO2,故③错误;
④1molCu参加反应生成+1价铜离子,有1mol电子发生转移,故④正确,
故答案为:1s22s22p63s23p63d104s1;③;
(5)Z为Cu元素,铜原子位于顶点和面心,每个晶胞中含有铜原子的数目为:8×$\frac{1}{8}$+6×$\frac{1}{4}$=4,晶胞中含有4个铜原子,则晶胞的质量为:$\frac{64×4}{{N}_{A}}$g,设该晶胞的边长为xcm,则该晶胞体积为:x3cm3,则::$\frac{64×4}{{N}_{A}}$g=x3cm3×9.00g/cm3,整理可得x=$\root{3}{4.72×1{0}^{-23}}$;
SO42-离子的中心原子S的价层电子对为:4+$\frac{6+2-2×4}{2}$=4,孤电子对数为0,故其空间结构为正四面体,S原子杂化方式为:sp3,
故答案为:$\root{3}{4.72×1{0}^{-23}}$;正四面体;sp3.
点评 本题是对物质结构的考查,涉及核外电子排布、分子结构与性质、杂化方式、晶胞计算等,(5)中晶胞的计算为难点、易错点,难度中等.

| A. |  Mg作负极,电子流向:Mg一→稀硫酸一→A1 | |
| B. |  Al作负极,电极反应式6H2O+6e-═6OH-+3H2↑ | |
| C. |  Cu作负极,电极反应式Cu-2e-═Cu2+ | |
| D. |  Cu作正极,电极反应式:2H++2e═H2↑ |
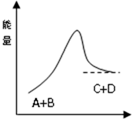
| A. | 铝与稀盐酸的反应符合该图示 | B. | 该反应为吸热反应 | ||
| C. | A的能量一定低于C的能量 | D. | 该反应只有在加热条件下才能进行 |

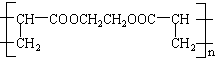 ,回答下列问题:
,回答下列问题: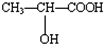 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$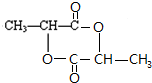 +2H2O.
+2H2O.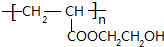 .
.
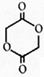 ;C中所含官能团的名称是羧基、溴原子.
;C中所含官能团的名称是羧基、溴原子.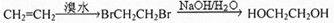 .
.