题目内容
19.如图所示的四个原电池装置,其中结论正确的是( )| A. |  Mg作负极,电子流向:Mg一→稀硫酸一→A1 | |
| B. |  Al作负极,电极反应式6H2O+6e-═6OH-+3H2↑ | |
| C. |  Cu作负极,电极反应式Cu-2e-═Cu2+ | |
| D. |  Cu作正极,电极反应式:2H++2e═H2↑ |
分析 A、根据在硫酸中金属镁比铝活泼是负极,电子不经过溶液;
B、根据在氢氧化钠中金属铝比镁活泼是负极,发生失电子氧化反应;
C、金属铁在常温下遇浓硝酸钝化,所以所以负极为铜,发生失电子氧化反应;
D、铁、铜、氯化钠构成的原电池中,金属铁发生的是吸氧腐蚀.
解答 解:A、在硫酸中金属镁比铝活泼,失电子的是金属镁,为负极,但电子不经过溶液,故A错误;
B、在氢氧化钠中金属铝比镁活泼,失电子的是金属铝,为负极,电极反应式为Al+4OH--3e-═AlO2-+2H2O,故B错误;
C、金属铁在常温下遇浓硝酸钝化,所以负极为铜,电极反应式Cu-2e-═Cu2+,故C正确;
D、铁、铜、氯化钠构成的原电池中,金属铁为负极,金属铜为正极,铁发生的是吸氧腐蚀,正极上是氧气得电子的过程,故D错误.
故选C.
点评 本题考查学生原电池的工作原理知识,可以根据所学内容来回答,难度不大.

练习册系列答案
相关题目
9.通过核磁共振氢谱可以推知CH3CH2OH有多少种环境的氢原子( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
10.下列关于平衡常数的说法正确的是( )
| A. | 一定温度下的可逆反应,只有达到平衡时才具有平衡常数 | |
| B. | 化学平衡移动时,平衡常数一定改变 | |
| C. | 对于一个确定的反应来说,平衡常数的数值越大,反应限度越大 | |
| D. | 化学平衡常数大的可逆反应,所有反应物的转化率一定大 |
7.下面各种能量的转化,其本质属于光能--化学能转换的是( )
| A. | 太阳能热水器、反射式太阳灶 | |
| B. | 太阳能电池 | |
| C. | 利用生活垃圾中生物质能焚烧发电 | |
| D. | 通过植物的光合作用,产生生物质能 |
11.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | pH=1的稀硫酸中含有的H+数为0.1NA | |
| B. | 1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA | |
| C. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| D. | 80g NH4NO3晶体中含有NH4+小于个NA |
8.已知A、B、C、D、E、F、G是七种原子序数依次增大的短周期元素,它们的原子结构特征或有关物质的性质等如表所示.
(1)元素F在元素周期表中的位置是第三周期ⅥA族.这七种元素中,不属于主族元素的元素的名称是氖.
(2)在E、F、G三种元素中,原子半径最小的是Cl(填元素符号).
(3)元素A与G可形成化合物AG4,在该化合物中含有的化学键类型为共价键,分子的空间结构为正四面体.A与氧元素可形成化合物AO2,该化合物分子的电子式为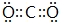 .
.
(4)元素B能与氢元素形成化合物BH3,在通常状况下,BH3的水溶液呈碱(填“酸”、“碱”或“中”)性,原因为NH3•H2O NH4++OH-(用方程式表示)
NH4++OH-(用方程式表示)
| 元素 | 原子结构特征或有关物质的性质 |
| A | 原子的最外层电子数是其内层电子数的2倍 |
| B | 其单质是空气中含量最多的物质 |
| C | 原子的最外层电子数是其电子层数的4倍 |
| D | 位于第ⅡA族,其原子半径比E的大 |
| E | 是金属元素,其氧化物和氢氧化物都有两性,且与D在同一周期 |
| F | 原子序数16,其单质在通常状况下为固体 |
| G | 原子的最外层电子数比其次外层电子数少1个 |
(2)在E、F、G三种元素中,原子半径最小的是Cl(填元素符号).
(3)元素A与G可形成化合物AG4,在该化合物中含有的化学键类型为共价键,分子的空间结构为正四面体.A与氧元素可形成化合物AO2,该化合物分子的电子式为
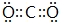 .
.(4)元素B能与氢元素形成化合物BH3,在通常状况下,BH3的水溶液呈碱(填“酸”、“碱”或“中”)性,原因为NH3•H2O
 NH4++OH-(用方程式表示)
NH4++OH-(用方程式表示)
9.由氧化铜、氧化铁组成的混合物ag,加入2mol•L-1的硫酸50mL时固体恰好完全溶解.若将ag该混合物在足量的一氧化碳中加热充分反应,冷却后固体质量减少为( )
| A. | 1.6g | B. | (a-1.6)g | C. | (a-3.2)g | D. | 无法计算 |
 A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题: