题目内容
18.某烃A不能使酸性KMnO4溶液褪色,0.5molA完全燃烧时,得到1.5mol水和67.2L(标准情况下)二氧化碳.(1)A的结构简式为
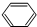 .
.(2)根据下列条件写出有关反应的化学方程式:
①A与足量H2在一定条件下发生反应生成C:
 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$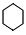
②在催化剂FeCl3作用下,A与Cl2反应生成
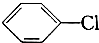 :
: +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$ +HCl.
+HCl.
分析 0.5mol A完全燃烧时,得到1.5mol水和67.2L二氧化碳,二氧化碳物质的量为$\frac{67.2L}{22.4L/mol}$=3mol,则烃A分子中C原子数目为$\frac{3mol}{0.5mol}$=6、H原子数目为$\frac{1.5mol×2}{0.5mol}$=6,故烃分子式为C6H6,烃A不能使溴水褪色,则烃A为 ,苯可以与氢气发生加成反应,与氯气发生取代反应,以此解答该题.
,苯可以与氢气发生加成反应,与氯气发生取代反应,以此解答该题.
解答 解:(1)0.5mol A完全燃烧时,得到1.5mol水和67.2L二氧化碳,二氧化碳物质的量为$\frac{67.2L}{22.4L/mol}$=3mol,则烃A分子中C原子数目为$\frac{3mol}{0.5mol}$=6、H原子数目为$\frac{1.5mol×2}{0.5mol}$=6,故烃分子式为C6H6,烃A不能使溴水褪色,则烃A为 ,
,
故答案为: ;
;
(2)①在催化剂作用下A与H2反应生成C,反应方程式为: +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$ ,
,
故答案为: +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$ ;
;
②在催化剂FeCl3的作用下,A与Cl2反应生成 ,反应方程式为:
,反应方程式为: +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$ +HCl,
+HCl,
故答案为: +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$ +HCl.
+HCl.
点评 本题考查有机物分子式确定、苯的性质等,为高频考点,侧重于学生的分析能力的考查,难度不大,注意掌握常见有机物的结构与性质.

练习册系列答案
相关题目
8.下列说法正确的是( )
| A. | 硅石常用作光导纤维、光学仪器的原料 | |
| B. | Al(OH)3可作阻燃剂,因此可以用于灭火 | |
| C. | 酚醛树脂可作木材粘合剂、制作食用器具 | |
| D. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 |
9.下列实验操作对应的实验现象及解释或结论都正确的是( )
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 用某无色溶液进行焰色反应 | 焰色呈黄色 | 原溶液一定是钠盐溶液 |
| B | 向NaOH溶液中滴加足量的MgCl2 溶液,然后再滴加足量的CuCl2溶液 | 先产生白色沉淀, 然后沉淀变蓝色 | KSP[Cu(OH)2]>KSP[Mg(OH)2] |
| C | 将水蒸汽通过灼热的铁粉 | 粉末变红 | 铁与水蒸汽在高温下发生 反应 |
| D | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2(g)═N2O4(g) △H<0 |
| A. | A | B. | B | C. | C | D. | D |
6.常温下,某无色溶液用激光笔照射无丁达尔现象,加入FeCl3后溶液显色.下列各组微粒在此溶液可以大量共存的是( )
| A. | Na+、K+、Fe2+、Cl- | B. | K+、Fe3+、NO3-、Fe(OH)3(胶体) | ||
| C. | Cl-、SCN-、NH4+、葡萄糖分子 | D. | OH-、Na+、苯酚、Br - |
13.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,11.2 L SO3所含的氧原子数为1.5NA | |
| B. | 电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA | |
| C. | 常温常压下,7.8 gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8 NA | |
| D. | 在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
3.工业上用软锰矿和闪锌矿联合生产MnO2和Zn的化学方程式为:
①MnO2+ZnS+2H2SO4$\frac{\underline{\;电解\;}}{\;}$MnSO4+ZnSO4+S+2H2O
②MnSO4+ZnSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$MnO2+Zn+2H2SO4.
下列说法中错误的是( )
①MnO2+ZnS+2H2SO4$\frac{\underline{\;电解\;}}{\;}$MnSO4+ZnSO4+S+2H2O
②MnSO4+ZnSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$MnO2+Zn+2H2SO4.
下列说法中错误的是( )
| A. | 反应①中MnO2和H2SO4都是氧化剂 | |
| B. | 反应①中每析出12.8g S沉淀,转移0.8mol电子 | |
| C. | 金属锌也可用热还原法制备 | |
| D. | 硫酸在生产种可循环使用 |
12.将51.2g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物,这些气体恰好被500mL 2.0mol/L NaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO2的物质的量是( )
| A. | 0.2 mol | B. | 0.4 mol | C. | 0.6 mol | D. | 0.8 mol |