题目内容
(2010?德阳模拟)[化学选修2:化学与技术]工业上为了使原料和能量得到充分的利用,常常采用循环操作.
Ⅰ、利用热化学循环制氢能缓解能源矛盾.最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢.MnFe2O4的制备:
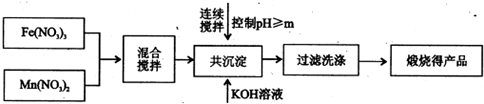
已知Fe3+、Mn2+沉淀的pH如表所示.
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比应为
(2)控制pH的操作中m的值为
Ⅱ、用MnFe2O4热化学循环制取氢气:MnFe2O4(s)
MnFe2O(4-x)(s)+
8O2(g);△H1=akJ/mol,
MnFe2O(4-x)(s)+xH2O(l)═MnFe2O4(s)+xH2(g);△H2=bkJ/mol,
(3)由上可知,H2燃烧的热化学方程式是
(4)该热化学循环制取氢气的优点是
A.过程简单、无污染 B.物料可循环使用 C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl通过如图的循环流程制取太阳能材料高纯硅.
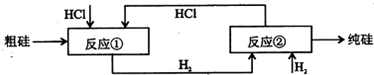
反应①Si(粗)+3HCl(g)
SiHCI3(l)+H2(g)
反应②:SiHCl3(l)+H2(g)
Si(纯)+3HCl(g)
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%.则在下一轮次的生产中,需补充投入HCl和H2的体积比是
Ⅰ、利用热化学循环制氢能缓解能源矛盾.最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢.MnFe2O4的制备:

已知Fe3+、Mn2+沉淀的pH如表所示.
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
2:1
2:1
.(2)控制pH的操作中m的值为
10.4
10.4
.Ⅱ、用MnFe2O4热化学循环制取氢气:MnFe2O4(s)
| ||
| x |
| 2 |
MnFe2O(4-x)(s)+xH2O(l)═MnFe2O4(s)+xH2(g);△H2=bkJ/mol,
(3)由上可知,H2燃烧的热化学方程式是
H2(g)+
O2(g)═H2O(l);△H=-
kJ/mol
| 1 |
| 2 |
| a+b |
| x |
H2(g)+
O2(g)═H2O(l);△H=-
kJ/mol
.| 1 |
| 2 |
| a+b |
| x |
(4)该热化学循环制取氢气的优点是
A、B、C
A、B、C
(填字母编号).A.过程简单、无污染 B.物料可循环使用 C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl通过如图的循环流程制取太阳能材料高纯硅.

反应①Si(粗)+3HCl(g)
| ||
反应②:SiHCl3(l)+H2(g)
| ||
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%.则在下一轮次的生产中,需补充投入HCl和H2的体积比是
3:1
3:1
.分析:(1)复合氧化物铁酸锰(MnFe2O4)的化学式确定理论上投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比;
(2)根据表中数据Mn2+完全沉淀的PH可知控制pH的操作中m的值;
(3)利用盖斯定律将两热化学方程式相加之后可得水分解的热化学方程式,即可确定H2燃烧的热化学方程式;
(4)该热化学循环制取氢气的优点是过程简单、无污染、物料可循环使用、氧气和氢气在不同步骤生成,安全且易分离;
(5)根据反应物和生成物的物质的量关系可确定需补充投入HCl和H2的体积比.
(2)根据表中数据Mn2+完全沉淀的PH可知控制pH的操作中m的值;
(3)利用盖斯定律将两热化学方程式相加之后可得水分解的热化学方程式,即可确定H2燃烧的热化学方程式;
(4)该热化学循环制取氢气的优点是过程简单、无污染、物料可循环使用、氧气和氢气在不同步骤生成,安全且易分离;
(5)根据反应物和生成物的物质的量关系可确定需补充投入HCl和H2的体积比.
解答:解:(1)铁酸锰的化学式为MnFe2O4,理论上投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比2:1,故答案为:2:1
(2)Mn2+完全沉淀的PH为10.4,控制pH的操作中m的值应为10.4,故答案为:10.4;
(3)利用盖斯定律计算:
MnFe2O4(s)
MnFe2O(4-x)(s)+
O2(g);△H1=akJ/mol…①,
MnFe2O(4-x)(s)+xH2O(1)═MnFe2O4(s)+xH2(g);△H2=bkJ/mol…②,
根据氢气燃烧的方程式H2+
O2═H2O可知热化学方程式为:H2(g)+
O2(g)═H2O(l);△H=-
=-
kJ/mol,
故答案为:H2(g)+
O2(g)═H2O(l);△H=-
kJ/mol;
(4)制备过程无污染,生成气体为氢气和氧气,MnFe2O4可循环使用,产品易于分离,且生产安全,
故答案为:A、B、C;
(5)反应①中每消耗3molHCl生成1molH2,而反应①中HCl的利用率和反应②中H2的利用率均为75%,所以反应后剩余的HCl和H2的体积比为3:1,则在下一轮次的生产中,需补充投入HCl和H2的体积比是3:1,故答案为:3:1.
(2)Mn2+完全沉淀的PH为10.4,控制pH的操作中m的值应为10.4,故答案为:10.4;
(3)利用盖斯定律计算:
MnFe2O4(s)
| ||
| x |
| 2 |
MnFe2O(4-x)(s)+xH2O(1)═MnFe2O4(s)+xH2(g);△H2=bkJ/mol…②,
根据氢气燃烧的方程式H2+
| 1 |
| 2 |
| 1 |
| 2 |
| ①+② |
| x |
| a+b |
| x |
故答案为:H2(g)+
| 1 |
| 2 |
| a+b |
| x |
(4)制备过程无污染,生成气体为氢气和氧气,MnFe2O4可循环使用,产品易于分离,且生产安全,
故答案为:A、B、C;
(5)反应①中每消耗3molHCl生成1molH2,而反应①中HCl的利用率和反应②中H2的利用率均为75%,所以反应后剩余的HCl和H2的体积比为3:1,则在下一轮次的生产中,需补充投入HCl和H2的体积比是3:1,故答案为:3:1.
点评:本题考查较为综合,涉及物质的制备和热化学方程式等问题,考查学生的评价能力,做题时注意考虑质量守恒选择原料的理论配比数.

练习册系列答案
相关题目