题目内容
11.某烯烃分子式为C6H12,其同分异构体中主链为4个碳原子的有( )| A. | 4种 | B. | 3种 | C. | 5种 | D. | 2种 |
分析 根据减碳法作取代基,书写C6H12主链上有4个碳原子的同分异构体,据此解答.
解答 解:分子式为C6H12且属于烯烃的主链为4个碳原子的同分异构体,若只含有一个支链,即剩余2个碳形成乙基,结构简式为: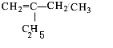 ,若为2个支链,则有2个甲基,分别为:
,若为2个支链,则有2个甲基,分别为: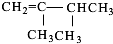 、
、 、
、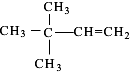 ,由于这四种烯烃均不存在顺反异构,故总共有4种结构,
,由于这四种烯烃均不存在顺反异构,故总共有4种结构,
故选:A.
点评 本题考查同分异构体的书写,难度不大,侧重对基础知识的巩固,注意掌握烯烃同分异构体的书写方法.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
1.拟用如图装置制取如下表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热,a、b、c、d表示相应仪器中加入的试剂).能达到实验目的是( )
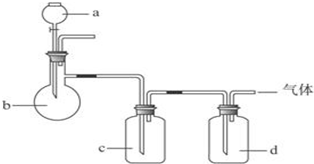

| 选项 | 气体 | a | b | c | d |
| A | SO2 | 硫酸 | 亚硫酸钠 | 浓硫酸 | NaOH溶液 |
| B | NH3 | 浓氨水 | 消石灰 | 浓硫酸 | H2O |
| C | O2 | 双氧水 | MnO2 | H2O | 浓硫酸 |
| D | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
2.有5种短周期元素在周期表中位置如图所示.已知:X的氢化物可用于刻蚀普通玻璃.下列推断正确的是( )
| | | G | | X |
| R | T | Y |
| A. | R和Y组成的化合物水溶液呈中性 | |
| B. | 最高价氧化物的水化物酸性:Y>G>X>R | |
| C. | 简单氢化物稳定性:X>Y>T | |
| D. | 常温下,TX4、TY4都呈液态 |
19.室温下,将1molNa2CO3•10H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1molNa2CO3(s)溶于水会使溶液温度升高,热效应为△H2;Na2CO3•10H2O受热分解的化学方程为:Na2CO3•10H2O(s)$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3(s)+10H2O(l),热效应为△H3,则下列判断正确的是( )
| A. | △H2<△H3 | B. | △H1>△H3 | C. | △H1+△H3=△H2 | D. | △H1+△H2>△H3 |
6.将2molA与2molB混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)?2C(g)+xD(g),2min后达到平衡时,A的转化率为50%,测得v(D)=0.25mol/(L•min).下列推断正确的是( )
| A. | v(C)=0.5mol/(L•min) | B. | x=3 | ||
| C. | B的转化率为25% | D. | 平衡时C的体积分数为28.6% |
16.下列关于化学键的叙述,正确的一项是( )
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均存在化学键 | |
| C. | 含有非极性共价键的分子一定是单质分子 | |
| D. | 含有共价键的化合物一定是共价化合物 |
3.下列有关元素锶(38Sr,ⅡA族)的叙述最不可能的是( )
| A. | 其氯化物是离子化合物 | B. | 其最高价氧化物水化物为一种弱碱 | ||
| C. | 它比Ca更易置换水中的氢 | D. | 它的碳酸盐难溶于水 |
20.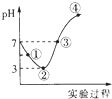 常温下,将Cl2缓慢通入100mL的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
常温下,将Cl2缓慢通入100mL的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
 常温下,将Cl2缓慢通入100mL的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )
常温下,将Cl2缓慢通入100mL的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是( )| A. | ①处c(H+)约为②处c(H+)两倍 | |
| B. | 曲线③④段有离子反应:HClO+OH-═H2O+ClO- | |
| C. | 可以依据②处数据计算所得溶解的氯气的量n(Cl2) | |
| D. | ③处表示氯气与氢氧化钠恰好反应完全 |
12.甲、乙两个容器内都在进行A→B的反应,甲中每分钟减少4mol A,乙中每分钟减少2mol A,则两容器中的反应速率( )
| A. | 甲快 | B. | 乙快 | C. | 相等 | D. | 无法确定 |