题目内容
(2011?中山三模)下列有关物质性质的比较正确的是( )
分析:A、同主族元素从上到下,非金属性减弱,金属性增强.单质的熔点非金属族增大,金属族降低;
B、主族元素正化合价数等于它的族序数,但氟元素、氧元素一般没有正化合价;
C、同一主族的气态氢化物水溶液的酸性一般是非金属性强的酸性弱,非金属性弱的酸性强;同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;
D、非金属性越强,最高价氧化物对应水化物的酸性越强.
B、主族元素正化合价数等于它的族序数,但氟元素、氧元素一般没有正化合价;
C、同一主族的气态氢化物水溶液的酸性一般是非金属性强的酸性弱,非金属性弱的酸性强;同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;
D、非金属性越强,最高价氧化物对应水化物的酸性越强.
解答:解:A、同主族元素从上到下,非金属性减弱,金属性增强.单质的熔点非金属族增大,如卤族元素,金属族熔点降低,如碱金属,故A错误;
B、主族元素正化合价数等于它的族序数,但氟元素、氧元素一般没有正化合价,故B错误;
C、同一主族的气态氢化物水溶液的酸性一般来说,非金属性强的酸性弱,非金属性弱的酸性强,如:氟化氢,氯化氢,溴化氢,碘化氢,他们的水溶液酸性依次增强,可氟氯溴碘的非金属性却依次减弱;同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强,如:碳,氮,氧,氟.碳的氢化物,甲烷,不溶于水,氮的氢化物氨气的水溶液氨水则为碱性,氧的氢化物,水则为中性,氟的氢化物氟化氢则为酸性,故C错误;
D、同周期自左而右非金属性增强,所以非金属性Cl>S>P>Si,非金属性越强,最高价氧化物对应水化物的酸性越强,所以酸性HClO4>H2SO4>H3PO4>H2SiO3,故D正确.
故选D.
B、主族元素正化合价数等于它的族序数,但氟元素、氧元素一般没有正化合价,故B错误;
C、同一主族的气态氢化物水溶液的酸性一般来说,非金属性强的酸性弱,非金属性弱的酸性强,如:氟化氢,氯化氢,溴化氢,碘化氢,他们的水溶液酸性依次增强,可氟氯溴碘的非金属性却依次减弱;同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强,如:碳,氮,氧,氟.碳的氢化物,甲烷,不溶于水,氮的氢化物氨气的水溶液氨水则为碱性,氧的氢化物,水则为中性,氟的氢化物氟化氢则为酸性,故C错误;
D、同周期自左而右非金属性增强,所以非金属性Cl>S>P>Si,非金属性越强,最高价氧化物对应水化物的酸性越强,所以酸性HClO4>H2SO4>H3PO4>H2SiO3,故D正确.
故选D.
点评:本题考查元素周期律、同族元素性质递变规律等,难度不大,注意规律的理解掌握与特殊性.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
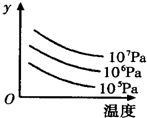 (2011?中山三模)某密闭容器中,可逆反应 L(s)+G(g)?3R(g);△H>0,如图表示外界条件温度、压强的变化对上述反应的影响.下列表述正确的是( )
(2011?中山三模)某密闭容器中,可逆反应 L(s)+G(g)?3R(g);△H>0,如图表示外界条件温度、压强的变化对上述反应的影响.下列表述正确的是( )