题目内容
(2011?中山三模)NA代表阿伏加德罗常数.下列有关叙述正确的是( )
分析:A、依据溶液的条件不是1L分析;
B、依据氦气是单原子分子分析判断;
C、质量换算物质的量,依据氧元素物质的量计算判断;
D、依据醋酸存在电离平衡,结合溶液中含有大量水分子分析.
B、依据氦气是单原子分子分析判断;
C、质量换算物质的量,依据氧元素物质的量计算判断;
D、依据醋酸存在电离平衡,结合溶液中含有大量水分子分析.
解答:解:A、NA个NH3分子气体溶于1L水,溶液体积不是1L,只有溶液的体积是1L其浓度才是1mol?L-1,故A错误;
B、氦气是单原子分子,标准状况下,11.2L氦气中约含有0.5NA个氦原子,故B错误;
C、32g含有少量臭氧的氧气中氧元素物质的量为
=2mol,共含有2NA个氧原子,故C正确;
D、醋酸是弱电解质,100mL0.1mol?L-1醋酸溶液含有醋酸分子小于0.01mol,溶液含有的分子总数包括水分子,所以分子总数大于0.01NA,故D错误;
故选C.
B、氦气是单原子分子,标准状况下,11.2L氦气中约含有0.5NA个氦原子,故B错误;
C、32g含有少量臭氧的氧气中氧元素物质的量为
| 32g |
| 16g/mol |
D、醋酸是弱电解质,100mL0.1mol?L-1醋酸溶液含有醋酸分子小于0.01mol,溶液含有的分子总数包括水分子,所以分子总数大于0.01NA,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的应用,主要是溶液体积的判断,稀有气体是单原子分子,元素守恒的计算,弱电解质的电离平衡.

练习册系列答案
相关题目
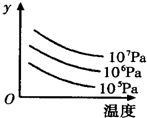 (2011?中山三模)某密闭容器中,可逆反应 L(s)+G(g)?3R(g);△H>0,如图表示外界条件温度、压强的变化对上述反应的影响.下列表述正确的是( )
(2011?中山三模)某密闭容器中,可逆反应 L(s)+G(g)?3R(g);△H>0,如图表示外界条件温度、压强的变化对上述反应的影响.下列表述正确的是( )