题目内容
【题目】关于化学反应,下列叙述中不正确的是 ( )
①放热的反应发生时不必加热 ②化学反应一定有能量变化 ③吸热反应需要加热后才能发生 ④化学反应热效应数值与参加反应的物质的量多少有关。
A. ②④B. ②③C. ①③D. ①②
【答案】C
【解析】
①一个化学反应发生的条件与反应的热效应无关;
②由于反应物、生成物具有的能量不同,化学反应中一定有能量变化;
③有的吸热反应不需要任何条件即可发生;
④参加反应的物质越多,反应热的数值就越大。
①放热的反应在常温下不一定很容易发生。如:铝热反应2Al+Fe2O3![]() Al2O3+2Fe是放热反应,但需在高热条件下以保证足够的热量引发氧化铁和铝粉反应,①错误;
Al2O3+2Fe是放热反应,但需在高热条件下以保证足够的热量引发氧化铁和铝粉反应,①错误;
②由于反应物、生成物具有的能量不同,化学反应中一定有能量变化,其表现形式有热量、光能和电能等,如木材燃烧,放出热量的同时发光,②正确;
③有的吸热反应不需要任何条件即可发生,如氯化铵和氢氧化钡晶体的反应,③错误;
④不论是吸热反应还是放热反应,反应热效应的数值均与参加反应的物质的多少有关。参加反应的物质越多,反应热的数值就越大,反之,越小,④正确;
故含量选项是C。

【题目】经检测某工厂的酸性废水中所含离子及其浓度如下表所示:
离子 | Fe3+ | Cu2+ | SO42- | Na+ | H+ |
浓度/(mol/L) | 2×10-3 | 1×10-3 | 1×10-2 | 2×10-3 |
(1)c(H+)=________mol/L。
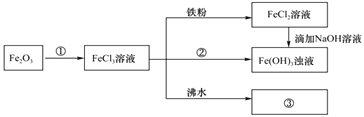
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4·7H2O).

① 工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+ =Fe2++Cu、________________、_________________。
②试剂B是__________。
③ 操作③是_____________、_____________、过滤,最后用少量冷水洗涤晶体,在低温下干燥。
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是__________________。
⑤ 获得的FeSO4·7H2O需密闭保存,原因是___________________________。若将所得FeSO4·7H2O配成溶液,向溶液中滴加NaOH溶液的现象是_________________________________________________________________。
⑥上述1000 L废水经处理,可获得 FeSO4·7H2O的物质的量是_________mol。