题目内容
【题目】“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
(1)硫酸工业排出的尾气(主要含SO2)有多种处理方式。
①写出用过量氨水吸收尾气的离子方程式:___________________。
②尾气也可用软锰矿浆(MnO2)吸收,写出如图所示“反应1”的化学方程式:___________________。

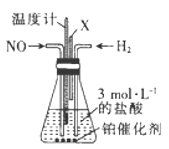
(2)治理汽车尾气中NO和CO的方法之一是在汽车的排气管上装一个催化转化装置,使NO和CO在催化剂作用下转化为无毒物质。写出该反应的化学方程式:___________________。
(3)某工厂拟综合处理含NH废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:

①“反应1”用于吸收Cl2,“反应1”的化学方程式为___________________。
② “反应2”的离子方程式为___________________。
【答案】 SO2+2NH3·H2O=2NH+SO![]() +H2O SO2+MnO2=MnSO4 2CO+2NO
+H2O SO2+MnO2=MnSO4 2CO+2NO![]() 2CO2+N2 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O NH+ NO
2CO2+N2 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O NH+ NO![]() =N2↑+2H2O
=N2↑+2H2O
【解析】(1)①硫酸工业尾气中的SO2用过量的氨水吸收反应生成亚硫酸铵,化学方程式为:SO2+2NH3·H2O=(NH4)2SO3+H2O,(NH4)2SO3为可溶性强电解质,书写离子方程式时拆成离子形式,故反应的离子方程式为:SO2+2NH3·H2O=2NH4++SO32-+H2O。②由图示可得,用软锰矿浆(MnO2)吸收SO2生成MnSO4,化学方程式为:SO2+MnO2=MnSO4。
(2)NO和CO在催化剂作用下转化为无毒物质,则发生氧化还原反应生成CO2和N2,故化学方程式为:2CO+2NO![]() 2CO2+N2。
2CO2+N2。
(3)①由流程结合已知,“反应1”用石灰乳吸收Cl2,故化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。②“反应2”为NH4+和NaNO2溶液反应生成无污染气体,根据氧化还原反应原理,NH4+和NO2-发生氧化还原反应生成N2,根据原子守恒还会生成H2O,该反应离子方程式为:NH4++NO2-=N2↑+2H2O。

 阅读快车系列答案
阅读快车系列答案【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测和处理.某工厂对制铬工业污泥中Cr(Ⅲ)的回收与再利用工艺如下(硫酸浸液中金属离子主要是Cr3+ , 其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+): 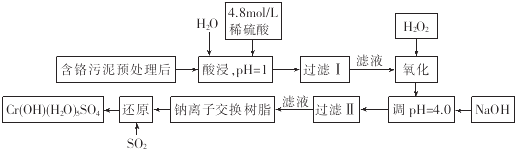
常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0 溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是(至少一条).
(2)调pH=4.0是为了除去
(3)钠离子交换树脂的作用原理为Mn++nNaR→MRn+nNa+ , 被交换的杂质离子是
(4)试配平下列氧化还原反应方程式:Fe2++H2O2+H+═Fe3++
(5)通入SO2的目的是 .