题目内容
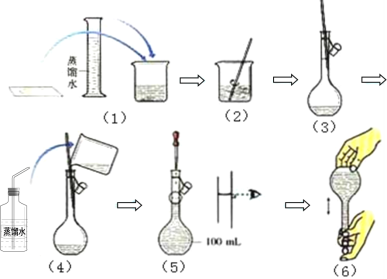
【题目】配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因有( )
A.NaOH固体放在滤纸上称量
B.NaOH固体中混有Na2O杂质
C.摇匀后发现液面低于刻度线,加水至刻度线
D.有少量NaOH溶液残留在烧杯中
【答案】B
【解析】
分析操作对n、V的具体影响,根据c=![]() 分析不当操作对浓度的影响。
分析不当操作对浓度的影响。
A、根据烧碱具有吸水性和腐蚀性,应放在小烧杯中称量,若放在纸上称量则会吸水,导致氢氧化钠的质量偏小,所配制的溶液浓度偏低,故A错误;
B、称量的NaOH固体中混有Na2O杂质,导致氢氧化钠物质的量偏大,溶液浓度偏高,故B正确;
C、摇匀后发现液面低于刻度线,加水至刻度线,会导致溶液体积偏大,浓度偏低,故C错误;
D、有少量NaOH溶液残留在烧杯中,导致氢氧化钠的物质的量偏小,浓度偏低,故D错误。
答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】现有三种可溶性物质A、B、C,其中A、B属于盐,C属于碱,它们溶于水后电离产生的所有离子如下表所示:
阳离子 | Na+ H+ Ba2+ |
阴离子 | OH- CO32- SO42- |
请根据下列叙述回答问题:
(1)C的化学式为___。
(2)A溶液与B溶液反应可生成气体,则该反应的离子方程式为___。
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为___,鉴别溶液中B的阴离子的试剂为___。
②D溶于稀硝酸的离子方程式为___。
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下体积为VL,则E在混合物中的质量分数的表达式为___。