��Ŀ����
����Ŀ���о�ͭ���仯��������ʶԿ��С�������������Ҫ�����壮
��1��ͭ�ɲ������·����Ʊ�
�ٻ���ͭ��Cu2S+O2![]() 2Cu+SO2
2Cu+SO2
��ʪ����ͭ��CuSO4+Fe�TFeSO4+Cu
�������ַ����У�ͭԪ�ؾ��� �����������ԭ������ͭ���ʣ����âٷ�ÿ�Ƶ�32gCu��ת�Ƶ��ӵ����ʵ����� ��
��2���ڳ�ʪ�Ŀ�����ͭ���Է����绯ѧ��ʴ������ͭ�̣�ͭ�̵Ļ�ѧʽΪ ������ʴ��������ӦʽΪ�� ����ͭ��п��ɵĻ�ͭ�Ͻ������⣬�����ʴ�ķ����� ��
��3����Li����CuO����ܷ�ӦΪ��2Li+CuO�TLi2O+Cu���������ҺΪ��������л���Һ����ص�������ӦʽΪ�� ����
��Cu2O��һ�ְ뵼����ϣ����ڼ�����Һ���õ�ⷨ��ȡ������ܷ�ӦʽΪ��
2Cu+H2O![]() Cu2O+H2����������ӦʽΪ�� ����Cu2OͶ��ϡ�����У��õ���ɫ��Һ�ͺ�ɫ������д���÷�Ӧ�����ӷ���ʽ�� ��
Cu2O+H2����������ӦʽΪ�� ����Cu2OͶ��ϡ�����У��õ���ɫ��Һ�ͺ�ɫ������д���÷�Ӧ�����ӷ���ʽ�� ��
��4��Ϊ�˻��մ�ͭ�������������е�Ag��Au��ijʵ��С��������й��������±���
��� | �����·�Ӧ | ��ѧƽ�ⳣ�� |
��Ӧ�� | Au+6HNO3Au��NO3��3+3NO2��+3H2O | ��10��5 |
��Ӧ�� | Au3++4Cl��[AuCl4]�� | ��105 |
�������п�֪�������½���������ᷴӦ����ȴ��������ˮ��Ũ������Ũ���������Ϊl��3�Ļ������������û�ѧƽ���ƶ�ԭ������Ҫ˵������������ˮ��ԭ�� ��
���𰸡���ԭ��1.5mol��Cu2��OH��2CO3��Cu2��OH��2CO3��O2+2H2O+4e��=4OH��������������������CuO+2e��+2Li+=Li2O+Cu��2Cu��2e��+2OH��=Cu2O+H2O��Cu2O+2H+=Cu2++Cu+H2O��Ũ���Ậ�д��������ӣ�Au3+�������������γ��ȶ���[AuCl4]�����ӣ�ʹ��Ӧ��ƽ�������ƶ�����Au������ˮ��
����������1��������Ӧ��CuԪ�ػ��ϼ���+2�ۻ�+2��ת��Ϊ0�ۣ�������ԭ��Ӧ������CuԪ�ر���ԭ�����âٷ�ÿ�Ƶ�32gCu��n��Cu��=![]() =0.5mol����Ҫ����ͭ�����ʵ���Ϊ0.25mol��ת�Ƶ��ӵ����ʵ���=0.25mol��[4������2��]=1.5mol��
=0.5mol����Ҫ����ͭ�����ʵ���Ϊ0.25mol��ת�Ƶ��ӵ����ʵ���=0.25mol��[4������2��]=1.5mol��
���Դ��ǣ���ԭ�� 1.5mol��
��2��Cu��������������̼��ˮ��Ӧ����Cu2��OH��2CO3 �� ����ͭ�̵Ļ�ѧʽΪCu2��OH��2CO3 �� �����������õ��Ӻ�ˮ��Ӧ�������������ӣ��缫��ӦʽΪO2+2H2O+4e��=4OH����Zn��Cu�͵���ʹ���ԭ��أ�Zn��ʧ���Ӷ���������Cu���������������������÷���Ϊ�������������������Դ��ǣ�
Cu2��OH��2CO3��O2+2H2O+4e��=4OH��������������������
��3����������CuO�õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪCuO+2e��+2Li+=Li2O+Cu�����Դ��ǣ�CuO+2e��+2Li+=Li2O+Cu��
��������ͭʧ���Ӻ����������ӷ�Ӧ����������ͭ��ˮ���缫��ӦʽΪ2Cu��2e��+2OH��=Cu2O+H2O��������ͭ��ϡ���ᷴӦ��������ͭ��Cu��ˮ�����ӷ���ʽΪCu2O+2H+=Cu2++Cu+H2O�����Դ��ǣ�2Cu��2e��+2OH��=Cu2O+H2O�� Cu2O+2H+=Cu2++Cu+H2O��
��4��Ũ���Ậ�д��������ӣ�Au3+�������������γ��ȶ���[AuCl4]�����ӣ�ʹ��Ӧ��ƽ�������ƶ�����Au������ˮ�У����Դ��ǣ�Ũ���Ậ�д��������ӣ�Au3+�������������γ��ȶ���[AuCl4]�����ӣ�ʹ��Ӧ��ƽ�������ƶ�����Au������ˮ�У�

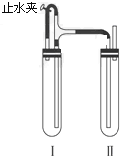
 ���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�����Ŀ������ʽ�ζ���ȷ��ȡ10.00mLijδ֪Ũ�ȵ���������һ�ྻ����ƿ�У�Ȼ����0.20molL ��1������������Һ��ָʾ��Ϊ��̪�����ζ�������£�
NaOH��ʼ���� | NaOH�յ���� | |
��һ�� | 0.50mL | 18.60mL |
�ڶ��� | 0.70mL | 19.00mL |
��1�������������ݿ��Լ������������ʵ���Ũ��ΪmolL��1 ��
��2���ﵽ�ζ��յ�ı�־�� ��
��3�����²�����ɲⶨ���ƫ�ߵ�ԭ������� �� A��δ�ñ�Һ��ϴ��ʽ�ζ���
B���ζ��յ����ʱ�����ӵζ��ܵĿ̶ȣ�������������ȷ
C��ʢװδ֪Һ����ƿ������ˮϴ����δ�ô���Һ��ϴ
D���ζ����յ����ʱ���ֵζ��ܼ��촦����һ����Һ��