题目内容
氯气和氮氧化物都是重要的化工原料,但进入大气后,都对环境造成污染。
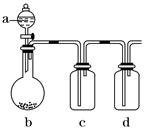
【Ⅰ】已知:2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+ 8 H2O,在实验室可用二氧化锰固体或高锰酸钾固体和浓盐酸反应制取氯气。可供选用的发生装置如下图。
(1)若用高锰酸钾固体和浓盐酸反应制取氯气,发生装置是 。(选填A或B或C)
(2)写出用二氧化锰固体和浓盐酸反应制取氯气的化学方程式: 。
(3)常用NaOH溶液吸收氯气防止污染。写出该反应的离子方程式 。
【Ⅱ】已知:NO2+NO+2NaOH=2NaNO2+H2O,可用氢氧化钠溶液可以吸收废气中的氮氧化物。
(1)在该反应中,氧化剂是 。
(2)汽车尾气中含有一氧化氮和一氧化碳,经过排气管中的催化转化器转化为对大气无污染的物质。写出该反应的化学方程式: 。
【Ⅰ】(1)B (2) 4HCl(浓)+MnO2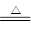 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(3) Cl2+2OH-=Cl-+ClO-+H2O
【Ⅱ】(1)NO2 (2) 2NO+2CO N2+2CO2
N2+2CO2
解析试题分析:【Ⅰ】(1)用高锰酸钾固体和浓盐酸反应制取氯气,依据题给反应的特征是固体和液体不加热制气体,选择发生装置B;(2)二氧化锰与浓盐酸在加热条件下反应生成二氯化锰、氯气与水,反应方程式为:4HCl(浓)+MnO2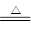 MnCl2+Cl2↑+2H2O(3)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O;
MnCl2+Cl2↑+2H2O(3)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O;
【Ⅱ】(1)反应NO2+NO+2NaOH═2NaNO2+H2O中,NO2中N元素化合价由+4价降低为NaNO2中的+3价,NO2是氧化剂;(2)一氧化氮和一氧化碳经过排气管中的催化转化器转化为对大气无污染的物质,应生成氮气、二氧化碳,反应方程式为:2NO+2CO N2+2CO2。
N2+2CO2。
考点:考查氯气的性质与实验室制备、氧化还原反应基本概念、化学方程式的书写

 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案制取下列气体,不宜采取排空气法收集的是( )
| A.氨气 | B.乙烯 | C.二氧化碳 | D.二氧化氮 |
下列气体既能用浓硫酸干燥又能用碱石灰干燥的是( )
| A.SO2 | B.NH3 | C.N2 | D.CO2 |
 2CaO+2S02↑+O2↑。
2CaO+2S02↑+O2↑。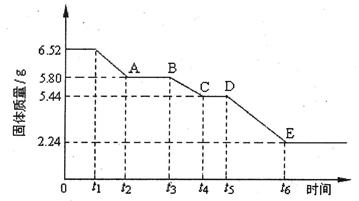


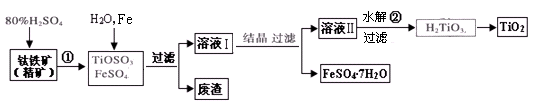
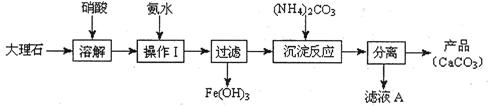
 价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下:
价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下:

 =
=

