题目内容
【题目】下图是实验室制备气体和验证气体性质的装置图,若利用该装置实现碳和浓硫酸的反应,并进行如下验证:

(1)实验步骤: 连接仪器、_________________、加药品后,然后滴入浓硫酸,加热。
(2)C与浓硫酸反应的化学方程式是___________________________。
(3)若要证明产物中的两种气体,装置B、C、D、E中分别装有品红溶液、酸性KMnO4溶液、品红溶液、澄清石灰水,则B、D装置中品红溶液的作用分别是________________,_________________。证明气体中有CO2的现象是____________________________。
(4)将A产生的气体通入下图装置(忽略氧气对反应的影响)进行如下探究实验。
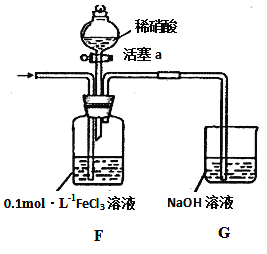
实验记录如下:
实验序号 | 实验操作 | 实验现象 |
I | 向F装置中通入一段时间的气体. | F中溶液色溶液最终变为浅绿色 |
II | 取出少量F装置中的溶液,先加入 KSCN溶液,再加入BaCl2溶液 | 加入KSCN溶液后溶液不变色;再加入BaCl2溶液产生白色沉淀. |
III | 打开活塞a,将过量稀HNO3加入装置F中,关闭活塞a | F中浅绿色溶液最终变为黄色. |
IV | 取出少量A装置中的溶液,加入KSCN溶液 | 溶液变为红色. |
实验II中发生反应的离子方程式是_____________________;实验III中,浅绿色溶液变为黄色的原因是___________________________________________ (用语言叙述);综合上述实验得岀的结论是:在酸性条件下,NO3﹣、Fe3+氧化性强弱顺序为_____________________
【答案】 检查装置气密性 C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O 验证SO2的存在 检验SO2是否除尽 D中品红不褪色,E中澄清石灰水变浑浊 Ba2++SO42﹣=BaSO4↓ 酸性条件下,NO3﹣把Fe2+氧化为Fe3+ NO3﹣>Fe3+
CO2↑+2SO2↑+2H2O 验证SO2的存在 检验SO2是否除尽 D中品红不褪色,E中澄清石灰水变浑浊 Ba2++SO42﹣=BaSO4↓ 酸性条件下,NO3﹣把Fe2+氧化为Fe3+ NO3﹣>Fe3+
【解析】试题分析:(1)实验室制备气体,连接仪器后要检验装置气密性。(2)C与浓硫酸反应生成二氧化碳、二氧化硫、水。
(3)若要证明产物中的两种气体, B装置中品红检验二氧化硫、C装置中酸性KMnO4溶液除去二氧化硫、D装置中品红检验二氧化硫是否除尽E装置中澄清石灰水检验二氧化碳。
(4)加入KSCN溶液后溶液不变色说明实验I中铁离子被还原为Fe2+,二氧化硫被氧化为SO42﹣,再加入BaCl2溶液产生硫酸钡沉淀;滴入硝酸,F中浅绿色溶液最终变为黄色,说明NO3﹣把Fe2+氧化为Fe3+;根据氧化还原反应规律判断NO3﹣、Fe3+氧化性强弱。
解析:(1)实验室制备气体,连接仪器后要检验装置气密性。
(2)C与浓硫酸反应生成二氧化碳、二氧化硫、水,反应方程式为C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(3)B装置中品红检验二氧化硫、C装置中酸性KMnO4溶液除去二氧化硫、D装置中品红检验二氧化硫是否除尽E装置中澄清石灰水检验二氧化碳。证明气体中有CO2的现象是D中品红不褪色,E中澄清石灰水变浑浊。
(4)加入KSCN溶液后溶液不变色说明实验I中铁离子被还原为Fe2+,二氧化硫被氧化为SO42﹣,再加入BaCl2溶液产生硫酸钡沉淀,反应离子方程式为Ba2++SO42﹣=BaSO4↓;滴入硝酸,F中浅绿色溶液最终变为黄色,说明NO3﹣把Fe2+氧化为Fe3+;氧化剂的氧化性大于氧化产物的氧化性,所以氧化性NO3﹣>Fe3+。

 名校课堂系列答案
名校课堂系列答案