题目内容
【题目】在体积都为1L,pH都等于2的盐酸和醋酸溶液中,投入0.65g锌粒,则下图所示比较符合客观事实的是( )
A.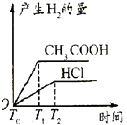
B.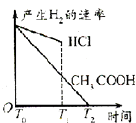
C.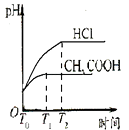
D.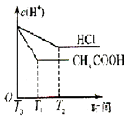
【答案】AC
【解析】解:体积都为1L,pH都等于2的盐酸和醋酸溶液中,n(CH3COOH)>n(HCl)=0.01mol,0.65g锌粒的物质的量= ![]() ,锌和酸反应Zn+2H+=Zn2++H2↑,盐酸酸溶液中氢离子不足,锌剩余0.005mol,醋酸溶液中存在电离平衡,平衡状态下的氢离子不足,但随着反应进行,醋酸又电离出氢离子进行反应,放出的氢气一定比盐酸多,开始时由于氢离子浓度相同,开始的反应速率相同,反应过程中醋酸溶液中的氢离子浓度始终比盐酸溶液中的氢离子浓度大,所以反应速率快;反应后,醋酸有剩余,导致醋酸溶液中pH小于盐酸溶液中;
,锌和酸反应Zn+2H+=Zn2++H2↑,盐酸酸溶液中氢离子不足,锌剩余0.005mol,醋酸溶液中存在电离平衡,平衡状态下的氢离子不足,但随着反应进行,醋酸又电离出氢离子进行反应,放出的氢气一定比盐酸多,开始时由于氢离子浓度相同,开始的反应速率相同,反应过程中醋酸溶液中的氢离子浓度始终比盐酸溶液中的氢离子浓度大,所以反应速率快;反应后,醋酸有剩余,导致醋酸溶液中pH小于盐酸溶液中;
A.产生氢气的量从0开始逐渐增多,最终由于醋酸电离平衡的存在,生成氢气的量比盐酸多,反应过程中氢离子浓度大于盐酸溶液中氢离子浓度,和同量锌反应速率快,故图象符合题意,故A正确;
B.反应开始氢离子浓度相同,反应速率相同.曲线从相同速率开始反应,但醋酸溶液中存在电离平衡,反应过程中醋酸溶液中的氢离子浓度始终比盐酸溶液中的氢离子浓度大,所以醋酸溶液反应过程中反应速率快,故B错误;
C.刚开始时,溶液的pH值为2,由于醋酸电离平衡的存在,反应过程中氢离子浓度大于盐酸溶液中氢离子浓度,所以醋酸反应速率始终大于盐酸反应速率,反应后,醋酸有剩余,导致反应过程中醋酸溶液pH始终小于盐酸溶液,故C正确;
D.反应开始氢离子浓度相同,反应过程中醋酸存在电离平衡,醋酸溶液中的氢离子浓度始终比盐酸溶液中的氢离子浓度大,故D错误;
故选AC.
根据盐酸和醋酸溶液中的氢离子物质的量和加入锌的物质的量,依据盐酸是强酸,醋酸是弱酸存在电离平衡判断反应过程和反应量的关系,结合图象中的纵坐标和横坐标的意义,曲线的变化趋势,起点、拐点、终点的意义分析判断是否符合事实.