题目内容
【题目】如图是一种综合处理SO2废气的工艺流程。若每步反应都完全,下列说法正确的是( )
(设反应过程中溶液的体积不变)
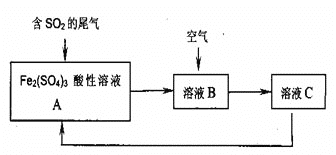
A.溶液B中发生的反应为:2SO2+O2→2SO3
B.由反应过程可推知氧化性:O2>Fe3+>SO42-
C.溶液的pH:A>B>C
D.A与C溶液成分相同,但浓度之比不同
【答案】BD
【解析】
A.溶液B中发生的反应是亚铁离子被氧气氧化为三价铁离子的反应,反应的离子方程式为:4Fe2++O2+4H+=4Fe3++2H2O,故A错误;
B.氧化还原反应中氧化剂的氧化性大于氧化产物,由反应2Fe3++2H2O+SO2=2Fe2++SO42﹣+4H+、4Fe2++O2+4H+=4Fe3++2H2O可知,氧化性O2>Fe3+>SO42﹣,故B正确;
C.反应过程中溶液的体积不变,溶液A为Fe2(SO4)3溶液,三价铁离子水解A溶液显酸性,溶液B为发生反应2Fe3++2H2O+SO2=2Fe2++SO42﹣+4H+后的溶液,溶液酸性大大增强;溶液C为硫酸铁溶液和硫酸溶液,由于发生反应为:4Fe2++O2+4H+=4Fe3++2H2O,消耗了氢离子,C的酸性大于A小于B,即三种溶液中氢离子浓度大小为:B>C>A,则溶液的pH大小为:A>C>B,故C错误;
D.溶液A中的溶质为硫酸和硫酸铁,溶液C的溶质也是硫酸铁、硫酸,不过C中硫酸的含量大于A,故D正确;
故答案为BD。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】1-乙氧基萘常用作香料,也可合成其他香料。实验室制备1-乙氧基萘的过程如下:
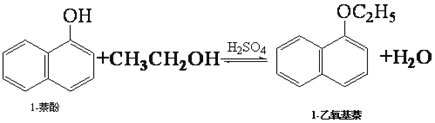
已知:1-萘酚的性质与苯酚相似,有难闻的苯酚气味。相关物质的物理常数:
物质 | 相对分子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
水 | 乙醇 | |||||
1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
(1)将72g 1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是________。
(2)装置中长玻璃管的作用是:______________。
(3)该反应能否用实验室制备乙酸乙酯的装置_____(选填“能”或“不能”),简述理由_____________。
(4)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是____________(选填编号)。

a.③②④① b.①②③④ c.②①③④
(5)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图所示,时间延长、温度升高,1-乙氧基萘的产量下降可能的两个原因是____________。

(6)提纯的产品经测定为43g,本实验中1-乙氧基萘的产率为________。